题目内容
(相对原子质量:H:1,O:16,Mg:24,Zn:65)
实验室用13g锌跟足量的稀硫酸反应,可制得氢气多少克?在标准状况下该气体为多少升?(标准状况下氢气密度为0.09g/L) (反应方程式:Zn+H2SO4═ZnSO4+H2↑)
实验室用13g锌跟足量的稀硫酸反应,可制得氢气多少克?在标准状况下该气体为多少升?(标准状况下氢气密度为0.09g/L) (反应方程式:Zn+H2SO4═ZnSO4+H2↑)
设生成氢气的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 2
13g x
=
解之得:x=0.4g.
这些气体的体积是
≈4.44L.
答:生成氢气的质量为0.4克,这些氢气在标准状况下的体积是4.44升.
Zn+H2SO4═ZnSO4+H2↑
65 2
13g x
| 65 |
| 2 |
| 13 |
| x |
解之得:x=0.4g.
这些气体的体积是
| 0.4g |
| 0.09g/L |
答:生成氢气的质量为0.4克,这些氢气在标准状况下的体积是4.44升.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
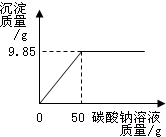
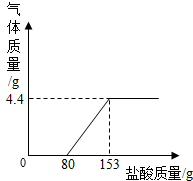 某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴滴加稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示.
某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴滴加稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示.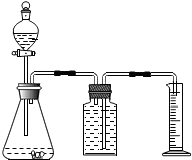 利用如图装置能制取氧气并测定所收集气体的体积.
利用如图装置能制取氧气并测定所收集气体的体积.