题目内容
某校化学兴趣小组从当地山上采集到一种石灰石,从中取出24g该样品,进行实验.
Ⅰ.将样品碾磨成粉末,放入一烧杯中;
Ⅱ.逐滴加入质量分数为10%的稀盐酸至不再产生气泡为止,共消耗该种稀盐酸146g.
请回答下列问题:
(1)将样品碾磨成粉末的目的是______.
(2)该实验中产生二氧化碳的质量为______g.
(3)该石灰石样品中碳酸钙的纯度是多少?(写出完整的计算过程)
解:(1)反应物接触面积越大,反应越完全,所以将样品碾磨成粉末使石灰石与稀盐酸反应更充分;
(2)设参加反应的碳酸钙的质量为x,生成二氧化碳的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x 146g×10% y
 =
=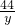
解得:x=20g,y=8.8g;
(3)石灰石中碳酸钙的纯度为 ×100%=83.3%.
×100%=83.3%.
答:该种石灰石中碳酸钙的纯度为83.3%.
分析:(1)反应物接触面积越大,反应越完全,可以据此解答;
(2)根据盐酸中氯化氢的质量结合化学方程式可以求算出二氧化碳的质量;
(3)根据盐酸中氯化氢的质量结合化学方程式可以求算出碳酸钙的质量,进而求算出碳酸钙的纯度.
点评:解答这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,然后根据所给的问题情景结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.
(2)设参加反应的碳酸钙的质量为x,生成二氧化碳的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x 146g×10% y
 =
=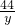
解得:x=20g,y=8.8g;
(3)石灰石中碳酸钙的纯度为
 ×100%=83.3%.
×100%=83.3%.答:该种石灰石中碳酸钙的纯度为83.3%.
分析:(1)反应物接触面积越大,反应越完全,可以据此解答;
(2)根据盐酸中氯化氢的质量结合化学方程式可以求算出二氧化碳的质量;
(3)根据盐酸中氯化氢的质量结合化学方程式可以求算出碳酸钙的质量,进而求算出碳酸钙的纯度.
点评:解答这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,然后根据所给的问题情景结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目




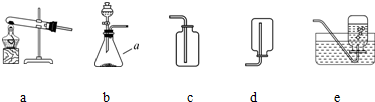


 排出,则该气体的密度比空气
排出,则该气体的密度比空气