题目内容
20. 如图是一瓶医用注射盐水标签的部分内容,请回答:
如图是一瓶医用注射盐水标签的部分内容,请回答:(1)H2O中H、O元素的质量比是1:8;
(2)氯化钠的相对分子质量是58.5;
(3)氯化钠中钠元素的质量分数是39.3%(精确到小数点后一位);
(4)该瓶盐水能给病人提供氯化钠的质量是4.5g;
(5)该瓶盐水能给病人提供钠元素的质量是1.8g(精确到0.1g)
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
(2)相对分子质量等于各元素相对原子质量之和;
(3)根据化合物中元素的质量分数计算方法来分析;
(4)根据医用注射盐水的密度、体积、溶质的质量分数进行分析解答即可;
(5)元素的质量=化合物的质量×化合物中该元素的质量分数.
解答 解:(1)水(H2O)中氢元素和氧元素的质量比(1×2):16=1:8.故填:1:8;
(2)氯化钠的化学式是NaCl,利用各元素原子量之和求相对分子质量,其相对分子质量=23+35.5=58.5.故填:58.5;
(3)氯化钠中钠元素的质量分数=$\frac{23}{58.5}×100%$≈39.3%.故填:39.3%;
(4)500mL=500cm3,由m=ρV,该瓶盐水的质量为1g/cm3×500cm3=500g;由溶质质量=溶液质量×溶质的质量分数,该瓶盐水能给病人提供氯化钠的质量是500g×0.9%=4.5g.故填:4.5;
(5)该瓶盐水能给病人提供钠元素的质量=4.5g×39.3%≈1.8g;故填:1.8g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.诗词是民族灿烂文化的瑰宝,下列诗句中含有物理变化的是( )
| A. | 夜来风雨声,花落知多少 | B. | 粉身碎骨浑不怕,要留清白在人间 | ||
| C. | 野火烧不尽,春风吹又生 | D. | 春蚕到死丝方尽,蜡炬成灰泪死干 |
11.对下列化学用语中数字“2”的说法正确的是
①2H ②2NH3 ③SO2 ④$\stackrel{+2}{Cu}$O ⑤Mg2+ ⑥2OH- ⑦H2O( )
①2H ②2NH3 ③SO2 ④$\stackrel{+2}{Cu}$O ⑤Mg2+ ⑥2OH- ⑦H2O( )
| A. | 表示分子中原子个数的是③⑦ | B. | 表示分子个数的是①② | ||
| C. | 表示离子个数的是⑤⑥ | D. | 表示离子所带电荷数的是④⑤ |
15.下列叙述正确的是( )
| A. | 分子、原子不显电性,故不显电性的粒子肯定是分子或原子 | |
| B. | 质子数相同的两种粒子其核外电子数一定相同 | |
| C. | 物理变化中分子种类不变,化学变化中分子种类改变 | |
| D. | 保持水的化学性质的最小粒子是氢原子和氧原子 |
10. 赵亮同学在实验室取用一定量的氢氧化钠(一种易潮解且强腐蚀性的药品),下面是他的称量过程.
赵亮同学在实验室取用一定量的氢氧化钠(一种易潮解且强腐蚀性的药品),下面是他的称量过程.
(1)调节天平平衡,静止时指针偏右,这时他应该怎么调整平衡螺母?向左调节平衡螺母
(2)用托盘天平称量一未知质量的烧杯.用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减去砝码.请用“↓”和“↑”在下表中表示他的称量过程,并用“|”表示游码在图中标尺上的位置(最终称得烧杯的实际质量为36.8g).
(3)该同学要称取8.5g氢氧化钠固体,他往左盘放入45g 砝码,并将游砝移至0.3g处,然后把烧杯放在右盘,向烧杯中加入药品至天平平衡为止,该同学认为他所称量的药品质量为45g+0.3g-36.8g=8.5g,如果你认为他的称量过程不正确那他所称量的药品实际质量是7.9克,如果你认为是正确此空不用填写.
 赵亮同学在实验室取用一定量的氢氧化钠(一种易潮解且强腐蚀性的药品),下面是他的称量过程.
赵亮同学在实验室取用一定量的氢氧化钠(一种易潮解且强腐蚀性的药品),下面是他的称量过程.(1)调节天平平衡,静止时指针偏右,这时他应该怎么调整平衡螺母?向左调节平衡螺母
(2)用托盘天平称量一未知质量的烧杯.用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减去砝码.请用“↓”和“↑”在下表中表示他的称量过程,并用“|”表示游码在图中标尺上的位置(最终称得烧杯的实际质量为36.8g).
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
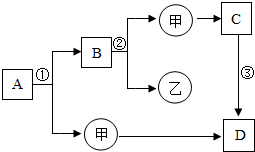 下列是初中化学常见物之间的转化关系,这些物质由碳、氢、氧元素组成的,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其余反应条件、部分反应物已略去.试推断:
下列是初中化学常见物之间的转化关系,这些物质由碳、氢、氧元素组成的,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其余反应条件、部分反应物已略去.试推断:

 甲、乙两位同学用如图所示的装置分别进行了实验探究.
甲、乙两位同学用如图所示的装置分别进行了实验探究.