题目内容
2.将H2、CO、CO2、N2依次通过足量下列物质:澄清石灰水、灼热的氧化铜、浓H2SO4(注:有吸水性),最终剩余的气体为( )| A. | N2 | B. | N2 CO2 | C. | H2 CO2 N2 | D. | N2 H2 |
分析 根据二氧化碳能与澄清石灰水反应,氢气和一氧化碳能与灼热的氧化铜反应,浓硫酸具有吸水性,据此进行分析判断即可.
解答 解:将H2、CO、CO2、N2通过澄清石灰水后,二氧化碳会与石灰水中的氢氧化钙反应生成碳酸钙和水,CO2被吸收;再通过灼热的氧化铜后,一氧化碳和氢气会与灼热的氧化铜反应分别生成铜和二氧化碳、铜和水,一氧化碳和氢气被吸收,但生成了二氧化碳和水蒸气;再通过浓硫酸除去水,最后剩余的气体为二氧化碳和氮气.
故选:B.
点评 本题难度不大,熟练掌握常见气体的性质是正确解答此类题的关键;解题时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
12.下列观点符合质量守恒定律的是( )
| A. | 一定条件下,CO和O2反应生成CO2,反应前后分子总数不变 | |
| B. | 铁钉在潮湿空气中一段时间后生锈,质量增加 了 | |
| C. | 某物质在空气中燃烧只生成CO2和H2O,则该物质一定由木炭、氢、氧三中元素组成 | |
| D. | 10克碳在10克氧气中充分燃烧生成20克二氧化碳 |
13.以下是KCl部分溶解度数据,下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
| A. | KCl饱和溶液中不能再溶解其他物质 | |
| B. | 20℃时,100g饱和KCl溶液中含KCl34.0g | |
| C. | 60℃时,将溶质质量分数为30%的KCl溶液降温至40℃,有晶体析出 | |
| D. | 20℃时,KCl溶液中溶质的质量分数一定小于40℃时KCl溶液中溶质的质量分数 |
8.正确进行化学实验操作十分重要,下列图示实验操作中正确的是( )
| A. |  读出液体体积 | B. |  过滤 | C. |  熄灭酒精灯 | D. |  取固体药品 |
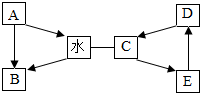 A-E是初中化学常见的物质.A和水具有相同的组成,D是大理石的主要成分,C、D、E 三种物质含有同种金属元素,A、C均属于氧化物,E是碱.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答:
A-E是初中化学常见的物质.A和水具有相同的组成,D是大理石的主要成分,C、D、E 三种物质含有同种金属元素,A、C均属于氧化物,E是碱.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答: 如图是初中化学实验的几种常用仪器,请按要求填空.
如图是初中化学实验的几种常用仪器,请按要求填空.
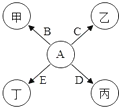 如图所示的是初中化学常见的四种物质,其中A、B、C、D、E是单质,甲、乙、丙、丁是氧化物,B和丙都是红色固体,E是最清洁的燃料,丙高温下可与乙反应可生成D(部分反应物、生成物及反应条件已略去).据此回答:
如图所示的是初中化学常见的四种物质,其中A、B、C、D、E是单质,甲、乙、丙、丁是氧化物,B和丙都是红色固体,E是最清洁的燃料,丙高温下可与乙反应可生成D(部分反应物、生成物及反应条件已略去).据此回答: