题目内容
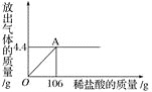
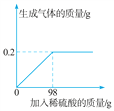
【题目】有一种石灰石样品(主要成分是CaCO3和SiO2)。课外小组同学将100g盐酸加入到30g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水。实验过程中溶液损失忽略不计),完全反应后测得烧杯中剩余物质质量是121.2g。请计算。
(1)反应后生成的二氧化碳的质量是___________。
(2)该石灰石样品中CaCO3的质量分数________________?(写出计算过程)
【答案】8.8 66.7%
【解析】
根据题意,利用烧杯中反应前后质量差,可求出二氧化碳的质量,再用二氧化碳的质量和化学方程式求出碳酸钙的质量,进一步计算出样品中碳酸钙的质量分数。
(1)依题意,反应后生成的二氧化碳的质量为:![]() 。
。
(2)解:设法该石灰石样品中CaCO3的质量为X。
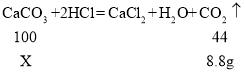
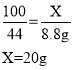
该石灰石样品中CaCO3的质量分数为:![]() 。
。
答:该石灰石样品中CaCO3的质量分数为66.7%。

练习册系列答案
相关题目
【题目】在化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。同学们对此气体展开了一系列探究。
(1)如果推测此气体是二氧化碳,验证它的实验方案如下:
猜想 | 实验步骤 | 现象与结论 |
此气体可能是CO2 | _____ | _____ |
产生此气体的化学方程式可能是_____;
(2)若想制取该气体,采用的发生装置可选取下图中的_____,收集装置应选用_____(填序号);
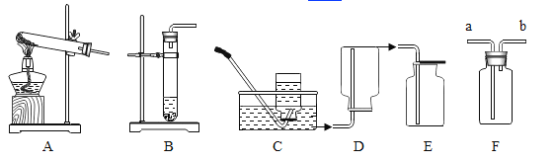
(3)如用下图中F装置收集该气体,气体应由_____端导入(填“a”或“b”)。