题目内容
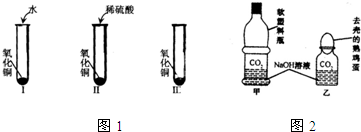
 氧化铜是一种黑色固体,可溶于稀硫酸中.巍巍想知道是硫酸中的H2O、H+、SO42-中的哪种粒子能使氧化铜溶解.请你和他一起设计实验来完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸中.巍巍想知道是硫酸中的H2O、H+、SO42-中的哪种粒子能使氧化铜溶解.请你和他一起设计实验来完成这次探究活动.
[提出假设]:______能使CuO溶解
[设计实验]:
(1)通过实验Ⅰ可以证明______;
(2)要证明另外两种粒子能否溶解氧化铜,还要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入______;
[结果分析]:通过实验可知:是稀硫酸中的______使氧化铜溶解.
[交流探讨]:根据实验结果,实验室中还有一种常用的试剂可以溶解氧化铜,它是______.
解:[提出假设]根据题给信息结合所学知识提出是氢离子使氧化铜溶解的假设;
[设计实验](1)实验I中加入的是水,所以可以证明水不能使氧化铜溶解;
(2)实验II中加入了稀硫酸,所以我们可以加入稀盐酸或是硫酸钠来做一个对比实验,以验证是氢离子还是硫酸根离子使氧化铜溶解的;
[结果分析]根据实验现象及对比实验可以知道是氢离子使氧化铜溶解的;
[交流讨论]根据所学知识可以判断盐酸、稀硝酸等也可以使氧化铜溶解.
故答案为:[提出假设]H+;
[设计实验](1)H2O不能使CuO溶解;
(2)盐酸(或Na2SO4溶液等);
[结果分析]:溶液中的H+使CuO溶解,H2O、SO42-不能使CuO溶解;
[交流讨论]:稀硝酸(或稀盐酸).
分析:[提出假设]根据所学知识及题给的信息,提出假设,然后进行验证;
[设计实验](1)实验I中加入的是水,实验I是验证水能否使氧化铜溶解;
(2)硫酸中含有硫酸根离子和氢离子,所以可以加入含有硫酸根离子的物质,或是含有氢离子的物质来进行对比实验;
[结果分析]通过对比实验结合所学知识可以得出结论;
[交流讨论]氧化铜可以溶于酸中,可以据此得出答案.
点评:知道金属氧化物可以和酸反应而生成盐和水,同时在探究问题时要学会使用控制变量法,通过对比可以较容易的得出正确的结论.
[设计实验](1)实验I中加入的是水,所以可以证明水不能使氧化铜溶解;
(2)实验II中加入了稀硫酸,所以我们可以加入稀盐酸或是硫酸钠来做一个对比实验,以验证是氢离子还是硫酸根离子使氧化铜溶解的;
[结果分析]根据实验现象及对比实验可以知道是氢离子使氧化铜溶解的;
[交流讨论]根据所学知识可以判断盐酸、稀硝酸等也可以使氧化铜溶解.
故答案为:[提出假设]H+;
[设计实验](1)H2O不能使CuO溶解;
(2)盐酸(或Na2SO4溶液等);
[结果分析]:溶液中的H+使CuO溶解,H2O、SO42-不能使CuO溶解;
[交流讨论]:稀硝酸(或稀盐酸).
分析:[提出假设]根据所学知识及题给的信息,提出假设,然后进行验证;
[设计实验](1)实验I中加入的是水,实验I是验证水能否使氧化铜溶解;
(2)硫酸中含有硫酸根离子和氢离子,所以可以加入含有硫酸根离子的物质,或是含有氢离子的物质来进行对比实验;
[结果分析]通过对比实验结合所学知识可以得出结论;
[交流讨论]氧化铜可以溶于酸中,可以据此得出答案.
点评:知道金属氧化物可以和酸反应而生成盐和水,同时在探究问题时要学会使用控制变量法,通过对比可以较容易的得出正确的结论.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
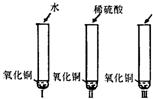 28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.
28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动. 21、氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过下图I、II、III三个实验完成这次探究活动.
21、氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过下图I、II、III三个实验完成这次探究活动.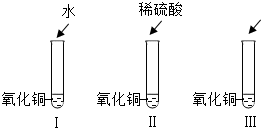 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.