题目内容
某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究.
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO
猜想二:是CaO和Ca(OH)2的混合物
猜想三:全部是Ca(OH)2
猜想四:是Ca(OH)2和CaCO3的混合物
【实验探究】(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含 .
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 .
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以上二种实验方案.写出方案二发生的化学反应方程式 .
【实验结论】通过以上实验探究,得出猜想 成立.
【拓展迁移】通过反思生石灰干燥剂变质的原因后,请判断下列气体中不能用生石灰作干燥剂的是 .(填序号) ①CO2②SO2③HCl ④NH3.
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO
猜想二:是CaO和Ca(OH)2的混合物
猜想三:全部是Ca(OH)2
猜想四:是Ca(OH)2和CaCO3的混合物
| 实验方案 | 方案一 | 方案二 |
| 实验操作 | 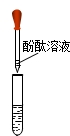 | 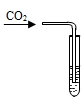 |
| 实验现象 | 溶液由无色变红色 | 澄清溶液变浑浊 |
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以上二种实验方案.写出方案二发生的化学反应方程式
【实验结论】通过以上实验探究,得出猜想
【拓展迁移】通过反思生石灰干燥剂变质的原因后,请判断下列气体中不能用生石灰作干燥剂的是
考点:实验探究物质的组成成分以及含量,生石灰的性质与用途,碱的化学性质,盐的化学性质
专题:科学探究
分析:【实验探究】(1)根据生石灰与水反应生成熟石灰放出大量热,可知一定不含生石灰进行解答;
(2)根据加足量酸有气泡,推断肯定含有碳酸盐,由此可以判断出该干燥剂中一定含有碳酸钙;
(3)根据二氧化碳与石灰水反应生成碳酸钙沉淀和水书写方程式;
【实验结论】:根据三个方案的实验探究,第一个方案通入二氧化碳变浑浊说明含有氢氧化钙,第二个实验方案指示剂的颜色变化肯定含有碱性物质,第三个方案也更说明含有氢氧化钙,由此得出猜想四是正确的;
【拓展迁移】能被生石灰来干燥的气体是与其不反应的气体.
(2)根据加足量酸有气泡,推断肯定含有碳酸盐,由此可以判断出该干燥剂中一定含有碳酸钙;
(3)根据二氧化碳与石灰水反应生成碳酸钙沉淀和水书写方程式;
【实验结论】:根据三个方案的实验探究,第一个方案通入二氧化碳变浑浊说明含有氢氧化钙,第二个实验方案指示剂的颜色变化肯定含有碱性物质,第三个方案也更说明含有氢氧化钙,由此得出猜想四是正确的;
【拓展迁移】能被生石灰来干燥的气体是与其不反应的气体.
解答:解:【实验探究】(1)加水没有发热现象,根据氧化钙(生石灰)溶于水放热的特性可以判断一定没有生石灰存在;故填:CaO;
(2)由于碳酸钙和盐酸反应放出二氧化碳气体,加入足量的酸有气泡产生说明该干燥剂中一定含有 CaCO3,但不能判断是否一定还有氢氧化钙,因Ca(OH)2 遇到酸不会有气泡产生,所以不能判定一定含有氢氧化钙;故填:CaCO3;
(3)常用澄清的石灰水来检验二氧化碳的存在,它会变浑浊说明含有氢氧化钙,反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;故填:Ca(OH)2+CO2═CaCO3↓+H2O;
【实验结论】:由以上实验探究得出猜想一,二,三都不可能有这几种情况的存在,所以猜想四成立;故填:四;
【拓展迁移】二氧化硫、二氧化碳和氯化氢气体均能与氧化钙反应,故不能用其干燥,而氨气不与氧化钙反应,可用其来干燥;故填:①②③.
(2)由于碳酸钙和盐酸反应放出二氧化碳气体,加入足量的酸有气泡产生说明该干燥剂中一定含有 CaCO3,但不能判断是否一定还有氢氧化钙,因Ca(OH)2 遇到酸不会有气泡产生,所以不能判定一定含有氢氧化钙;故填:CaCO3;
(3)常用澄清的石灰水来检验二氧化碳的存在,它会变浑浊说明含有氢氧化钙,反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;故填:Ca(OH)2+CO2═CaCO3↓+H2O;
【实验结论】:由以上实验探究得出猜想一,二,三都不可能有这几种情况的存在,所以猜想四成立;故填:四;
【拓展迁移】二氧化硫、二氧化碳和氯化氢气体均能与氧化钙反应,故不能用其干燥,而氨气不与氧化钙反应,可用其来干燥;故填:①②③.
点评:本题从生活中常见的食品干燥剂为情境角度出发,考查干燥剂是否变质,考查了学生对于CaO、Ca(OH )2、CaCO3 三者的性质的掌握和应用,尤其考查了学生在实验探究中推断分析能力.

练习册系列答案
相关题目
下列化学方程式书写正确的是( )
| A、Al+2HCl═AlCl2+H2↑ | ||||
B、KMnO4
| ||||
C、3CO+Fe2O3
| ||||
| D、Cu+FeSO4═CuSO4+Fe |
对下列物质的用途解释正确的是( )
| 物质用途 | 解 释 | |
| A | 石墨作电极 | 石墨具有优良导电性 |
| B | 二氧化碳用作气体肥料 | 二氧化碳既不燃烧也不支持燃烧 |
| C | 干冰用于人工降雨 | 干冰就是冰 |
| D | 用活性炭除去水中色素和异味 | 活性炭具有吸附性 |
| A、A | B、B | C、C | D、D |
 如图是甲、乙两种固体物质的溶解度曲线,据此判断下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,据此判断下列说法正确的是( )| A、将乙的饱和溶液降温,不能析出晶体 |
| B、t1℃时,甲、乙的溶解度相等 |
| C、t2℃时,30g乙加到100g水中能得到130g溶液 |
| D、升高温度,甲的不饱和溶液会变成饱和溶液 |
 “
“ ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种物质的分子,下图形象地表示了某化学反应前后反应物与生成物分子及其数目的变化.
”分别表示A、B、C三种物质的分子,下图形象地表示了某化学反应前后反应物与生成物分子及其数目的变化.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
| A、3:2:4 |
| B、3:2:2 |
| C、1:2:3 |
| D、1:2:2 |

 甲、乙、丙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.
甲、乙、丙是初中化学常见的物质,它们在一定条件下能如图所示相互转化. 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示: