题目内容
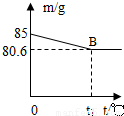 某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:
某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:(1)产生CO2的质量为______.
(2)该贝壳中CaCO3的质量分数.(结果保留至0.1%)
(3)所用稀盐酸的溶质质量分数.
【答案】分析:(1)碳酸钙和盐酸生成氯化钙和二氧化碳和水,所以反应前后质量差等于二氧化碳的质量.
(2)写出化学方程式并代入二氧化碳的质量即可计算出碳酸钙的质量,然后计算出贝壳中碳酸钙的质量分数.
(3)写出化学方程式并代入二氧化碳的质量即可计算出盐酸的质量,然后计算出盐酸中的溶质的质量分数.
解答:解:(1)根据题目信息可知,二氧化碳的质量=12克+73克-80.6克=4.4克,故答案为:4.4克.
(2)设贝壳中CaCO3的质量为X,参加反应的HCl的质量为Y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
X Y 4.4克
 ═
═
得:X=10克
 ═
═
得:Y=7.3克
∴贝壳中CaCO3的质量分数= ×100%═83.3%.
×100%═83.3%.
(3)有(1)计算可知,参加反应的盐酸(溶质)的质量是7.3克,由于“所用稀盐酸刚好消耗了加入量的一半”所以73克盐酸中的溶质的质量=7.3克×2═14.6克,则所用稀盐酸的溶质质量分数= ×100%═20%.
×100%═20%.
答:该贝壳中碳酸钙的质量分数为83.3%;盐酸溶液中溶质的质量分数为20%.
点评:掌握化学方程式的计算格式和规范性,本题的关键是知道二氧化碳的质量等于反应前后溶液的质量之差.
(2)写出化学方程式并代入二氧化碳的质量即可计算出碳酸钙的质量,然后计算出贝壳中碳酸钙的质量分数.
(3)写出化学方程式并代入二氧化碳的质量即可计算出盐酸的质量,然后计算出盐酸中的溶质的质量分数.
解答:解:(1)根据题目信息可知,二氧化碳的质量=12克+73克-80.6克=4.4克,故答案为:4.4克.
(2)设贝壳中CaCO3的质量为X,参加反应的HCl的质量为Y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
X Y 4.4克
 ═
═
得:X=10克
 ═
═
得:Y=7.3克
∴贝壳中CaCO3的质量分数=
 ×100%═83.3%.
×100%═83.3%.(3)有(1)计算可知,参加反应的盐酸(溶质)的质量是7.3克,由于“所用稀盐酸刚好消耗了加入量的一半”所以73克盐酸中的溶质的质量=7.3克×2═14.6克,则所用稀盐酸的溶质质量分数=
 ×100%═20%.
×100%═20%.答:该贝壳中碳酸钙的质量分数为83.3%;盐酸溶液中溶质的质量分数为20%.
点评:掌握化学方程式的计算格式和规范性,本题的关键是知道二氧化碳的质量等于反应前后溶液的质量之差.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
 某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:
某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算: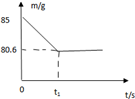 某兴趣小组测定贝壳中碳酸钙的含量.现取12克贝壳捣碎,放入烧杯中,然后向其中加入73克稀盐酸,充分反应.(贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应).测得烧杯中的反应剩余物的质量( m )与反应时间( t )的关系如图所示(忽略水蒸气的挥发),
某兴趣小组测定贝壳中碳酸钙的含量.现取12克贝壳捣碎,放入烧杯中,然后向其中加入73克稀盐酸,充分反应.(贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应).测得烧杯中的反应剩余物的质量( m )与反应时间( t )的关系如图所示(忽略水蒸气的挥发),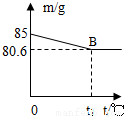 某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:
某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算: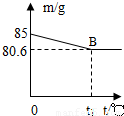 某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:
某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算: