题目内容
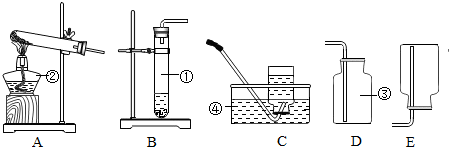
12. 实验验证质量守恒定律时,用电子天平和量筒准确测量出表中m1、m2和V,(实验中操作正确,O2的密度为ρg/cm3).
实验验证质量守恒定律时,用电子天平和量筒准确测量出表中m1、m2和V,(实验中操作正确,O2的密度为ρg/cm3).| 实验序号 | 1 | 2 | … |
| 加热前m1(试管+KMnO4)/g | |||
| 加热后m2(试管+剩余固体)/g | |||
| 量筒内收集气体的体积V/cm3 |
(2)装置中试管口略向下倾斜的原因是防止水蒸气冷凝回流到试管底部引起试管炸裂.
(3)作为KMnO4制氧气的装置,图中装置有何不足指出,请你指出试管口没有放置棉花团.
(4)当m1、m2、和V和ρ的等量关系为m1-m2=Vρ,说明此实验符合质量守恒定律.
分析 (1)根据化学反应的原理以及化学方程式的写法来分析;
(2)根据给试管中的固体加热的注意事项来分析;
(3)根据加热高锰酸钾制取氧气的注意事项来分析;
(4)根据质量守恒定律来分析解答.
解答 解:(1)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)给试管中的固体加热时试管口略向下倾斜的原因是:防止冷凝水倒流到热的试管底部而使试管破裂;故答案为:防止水蒸气冷凝回流到试管底部引起试管炸裂;
(3)加热高锰酸钾制取氧气时,为了防止高锰酸钾颗粒进入导气管,所以需要在试管口放置一棉花团;故填:试管口没有放置棉花团;
(4)在化学反应前后,物质的总质量不变,高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,则m1-m2=Vρ;故填:m1-m2=Vρ.
点评 本题考查了实验操作的注意事项、质量守恒定律及其应用等,难度稍大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20. 医院给病人输氧时用到类似如图的装置.关于该装置,下列说法中不正确的是( )
医院给病人输氧时用到类似如图的装置.关于该装置,下列说法中不正确的是( )
 医院给病人输氧时用到类似如图的装置.关于该装置,下列说法中不正确的是( )
医院给病人输氧时用到类似如图的装置.关于该装置,下列说法中不正确的是( )| A. | b导管连接供给氧气的钢瓶 | B. | b导管连接病人吸入氧气的塑料管 | ||
| C. | 使用该装置可使氧气变得湿润 | D. | 使用该装置来观察氧气输出的速率 |
7.如图是某反应的微观示意图,下列相关说法正确的是( )


| A. | C由三种元素组成 | B. | A和D中同种元素化合价不变 | ||
| C. | 该反应属于化合反应 | D. | 化学方程中B、C的分子个数比为1:1 |
17. 如图是钠的原子结构示意图.下列说法不正确的是( )
如图是钠的原子结构示意图.下列说法不正确的是( )
 如图是钠的原子结构示意图.下列说法不正确的是( )
如图是钠的原子结构示意图.下列说法不正确的是( )| A. | 钠属于金属元素 | B. | 钠离子的符号为Na+ | ||
| C. | 钠在化学反应中易得到电子 | D. | 钠原子的质子数为11 |
2.下列反应中属于化合反应的是( )
| A. | Fe+H2SO4═FeSO4+H2↑ | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | Na2O+H2O═2NaOH | D. | Na2SO4+BaCl2═BaSO4↓+2NaCl |