题目内容
二氧化碳和二氧化硫质量比1:1,求氧原子个数比 .
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:由题意,二氧化碳和二氧化硫质量比1:1,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,计算出氧元素的质量比;氧元素的质量比即为二氧化碳和二氧化硫中氧原子个数比.
解答:解:二氧化碳和二氧化硫质量比1:1,则含氧元素的质量比为(1×
×100%):(1×
×100%)=16:11;氧元素的质量比即为二氧化碳和二氧化硫中氧原子个数比,则氧原子个数比为16:11.
故答案为:16:11.
| 16×2 |
| 12+16×2 |
| 16×2 |
| 32+16×2 |
故答案为:16:11.
点评:本题难度不大,掌握化合物中某元素的质量=该化合物的质量×该元素的质量分数、氧元素的质量比即为氧原子个数比是正确解答本题的关键.

练习册系列答案
相关题目
在Mg食盐溶液中含有食盐mg,则该溶液的质量百分比浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|

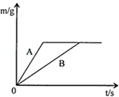 将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.
将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.