题目内容
(2011?石景山区二模)某品牌“钙片”标签上的部分内容如图所示.假设此钙片的其他成分不含钙元素也不与盐酸反应.为测定此钙片中的钙元素的含量,做了三次实验:取18片钙片放入盛有足量盐酸的容器中,充分反应后测得生成气体的质量和剩余物的质量,实验数据见下表.| 品牌:XX钙片 主要成分:碳酸钙 每瓶100片,重80g |
| 第1次 | 第2次 | 第3次 | 平均值 | |
| 钙片/片 | 18 | 18 | 18 | 18 |
| 生成气体的质量/g | 4.5 | 4.3 | 4.4 | 4.4 |
| 反应后剩余物质量/g | 83.1 | 83.0 | 82.9 | 83.0 |
(2)计算容器中盐酸的质量.
【答案】分析:(1)实验测量会出现误差,要取得接近准确值的方法一般是多次测量取平均值.根据二氧化碳的质量可求出碳酸钙的质量,根据碳酸钙的质量×碳酸钙中钙元素的质量分数求出钙元素的质量,最后根据 ×100%可求出钙片中钙元素的质量分数.
×100%可求出钙片中钙元素的质量分数.
(2)根据质量守恒定律,钙片的质量+稀盐酸的质量=反应后剩余物的质量+二氧化碳的质量,则稀盐酸的质量=反应后剩余物的质量+二氧化碳的质量-钙片的质量.
解答:解:(1)设钙片中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
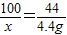
x=10g
钙元素的质量为:10g×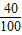 =4g
=4g
18片钙片的质量=80g× =14.4g
=14.4g
钙元素质量分数为: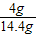 ×100%=27.8%
×100%=27.8%
(2)盐酸质量为:83g+4.4g-14.4g=73g
答:(1)钙片中钙元素的质量分数为27.8%.(2)容器中盐酸的质量为73g.
点评:本道题和我们一般所做的计算题有所不同,大多数计算题是让求反应后所得溶液的质量,而本题是让求所加盐酸的质量,依据的原理都是根据质量守恒定律,在计算反应后总物质质量时不能忽视了生成二氧化碳的质量.
 ×100%可求出钙片中钙元素的质量分数.
×100%可求出钙片中钙元素的质量分数.(2)根据质量守恒定律,钙片的质量+稀盐酸的质量=反应后剩余物的质量+二氧化碳的质量,则稀盐酸的质量=反应后剩余物的质量+二氧化碳的质量-钙片的质量.
解答:解:(1)设钙片中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
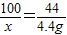
x=10g
钙元素的质量为:10g×
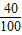 =4g
=4g18片钙片的质量=80g×
 =14.4g
=14.4g钙元素质量分数为:
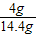 ×100%=27.8%
×100%=27.8%(2)盐酸质量为:83g+4.4g-14.4g=73g
答:(1)钙片中钙元素的质量分数为27.8%.(2)容器中盐酸的质量为73g.
点评:本道题和我们一般所做的计算题有所不同,大多数计算题是让求反应后所得溶液的质量,而本题是让求所加盐酸的质量,依据的原理都是根据质量守恒定律,在计算反应后总物质质量时不能忽视了生成二氧化碳的质量.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
 (2011?石景山区一模)A和B两种固体的溶解度曲线如右图所示.下列说法中,正确的是( )
(2011?石景山区一模)A和B两种固体的溶解度曲线如右图所示.下列说法中,正确的是( )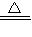 CO2↑+2SO2↑+2H2O.为了证明木炭与浓硫酸反应有二氧化碳和二氧化硫生成,甲、乙两位同学分别用下面的装置进行实验.实验中甲同学在C中盛放足量的饱和碳酸氢钠溶液,乙同学在C中盛放足量的酸性高锰酸钾溶液,两位同学在其他装置中盛放的药品相同且适量.
CO2↑+2SO2↑+2H2O.为了证明木炭与浓硫酸反应有二氧化碳和二氧化硫生成,甲、乙两位同学分别用下面的装置进行实验.实验中甲同学在C中盛放足量的饱和碳酸氢钠溶液,乙同学在C中盛放足量的酸性高锰酸钾溶液,两位同学在其他装置中盛放的药品相同且适量.
