题目内容
10. 有一包白色固体,可能由氯酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成.为探究该白色固体的组成.某小组学生取适量样品按如图所示流程进行实验,情回答下列问题.
有一包白色固体,可能由氯酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成.为探究该白色固体的组成.某小组学生取适量样品按如图所示流程进行实验,情回答下列问题.(1)写出试管滤液中的物质能与二氧化碳反应的化学方程式2KOH+CO2=K2CO3+H2O.
(2)白色沉淀Ⅱ的化学式为BaCO3.
(3)原白色固体中含有哪些物质?
分析 根据碳酸钙难溶于水,碳酸钙和盐酸反应会生成氯化钙、水和二氧化碳,氢氧化钾和二氧化碳反应生成碳酸钾,碳酸钾和氯化钡反应生成碳酸钡沉淀等知识进行分析.
解答 解:碳酸钙难溶于水,碳酸钙和盐酸反应会生成氯化钙、水和二氧化碳,氢氧化钾和二氧化碳反应生成碳酸钾,碳酸钾和氯化钡反应生成碳酸钡沉淀,
取样品加入适量的水溶解,得到的白色沉淀I中加入适量稀盐酸,白色沉淀完全溶解,所以样品中一定含有碳酸钙,滤液中通入二氧化碳也会生成白色沉淀II,所以样品中一定含有氢氧化钾、氯化钡,题中的现象不能确定是否含有氯酸钾,所以
(1)氢氧化钾和二氧化碳反应生成碳酸钾和水,化学方程式为:2KOH+CO2=K2CO3+H2O;
(2)通过推导可知,白色沉淀Ⅱ的化学式为:BaCO3;
(3)通过推导可知,原白色固体中含有:碳酸钙、氢氧化钾、氯化钡.
故答案为:(1)2KOH+CO2=K2CO3+H2O;
(2)BaCO3;
(3)碳酸钙、氢氧化钾、氯化钡.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列说法中不正确的是( )
| A. | 塑料、纤维、橡胶都属于有机合成材料 | |
| B. | 当人体缺乏维生素C时,会引起坏血病 | |
| C. | 生活中通过煮沸可以降低水的硬度 | |
| D. | 使用一些新型的、可降解的塑料是解决“白色污染”的有效措施之一 |
18. 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )| A. | 在0-a段发生3个化学反应 | |
| B. | c点的沉淀是BaSO4 | |
| C. | 图中m点的值是2.33 | |
| D. | 取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量 |
5.物质在“潮湿的空气”中发生变化与空气中某些气体有关.下列说法不正确的是( )
| A. | 钢铁生锈与氧气、水蒸气有关 | |
| B. | 氢氧化钠固体潮解、变质,与水蒸气、二氧化碳有关 | |
| C. | 铜器表面生成铜绿[Cu2(OH)2CO3]与O2、CO2、水蒸气有关 | |
| D. | 生石灰堆放久了变质与氧气有关 |
15.下列图示的实验操作正确的是( )
| A. | 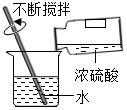 稀释浓硫酸 | B. | 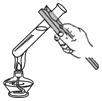 加热液体 | C. | 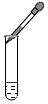 滴加少量液体 | D. | 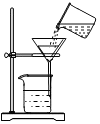 过滤 |
19.下列区分各组物质的两种方案都合理的是( )
| 选项 | A | B | C | D |
| 物质 | 碳酸钠和氢氧化钠 | 空气和氧气 | 尿素和硫酸铵 | 木炭和二氧化锰 |
| 方案一 | 稀盐酸 | 带火星的木条 | 氢氧化钠溶液 | 观察颜色 |
| 方案二 | 酚酞试液 | 燃烧的木条 | 加水 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
20.推理是化学学习中常用的思维方法,以下推理中正确的是( )
| A. | 酸与碱发生中和反应时生成盐和水,因此有盐和水生成的反应一定是中和反应 | |
| B. | 碱性溶液能使石蕊试液变蓝,能使石蕊试液变蓝的溶液一定呈碱性 | |
| C. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| D. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 |
