题目内容
取一定质量的碳酸钠和氯化钠的固体混合物,加入足量的稀盐酸至不再产生气泡为止,收集到二氧化碳气体的质量为4.4g,求该混合物中碳酸钠的质量________.
10.6g
分析:固体混合物中碳酸钠与盐酸反应放出二氧化碳,可利用产生二氧化碳的质量,根据反应的化学方程式,计算出样品中碳酸钠的质量;
解答:设固体混合物中碳酸钠的质量为x.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
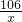 =
=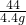 x=10.6g
x=10.6g
答:固体混合物中中碳酸钠的质量10.6g.
故答案为:10.6g
点评:根据化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算中反应中其它物质的质量.
分析:固体混合物中碳酸钠与盐酸反应放出二氧化碳,可利用产生二氧化碳的质量,根据反应的化学方程式,计算出样品中碳酸钠的质量;
解答:设固体混合物中碳酸钠的质量为x.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
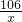 =
=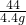 x=10.6g
x=10.6g答:固体混合物中中碳酸钠的质量10.6g.
故答案为:10.6g
点评:根据化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算中反应中其它物质的质量.

练习册系列答案
相关题目