题目内容
用炭粉还原氧化铜时,炭粉与氧化铜的质量比最好是( )
分析:根据碳和氧化铜反应的化学方程式,计算出炭粉与氧化铜的质量比(相对分子质量乘以化学计量数)即可.
解答:解:炭粉还原氧化铜生成铜和二氧化碳,反应的化学方程式为:C+2CuO
2Cu+CO2↑,
12 80×2
参加反应的炭粉与氧化铜的质量比12:(80×2)=3:40.
故选:C.
| ||
12 80×2
参加反应的炭粉与氧化铜的质量比12:(80×2)=3:40.
故选:C.
点评:本题难度不大,主要考查化学方程式中反应物质量比的计算,充分理解化学方程式的含义是正确解答本题的关键.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
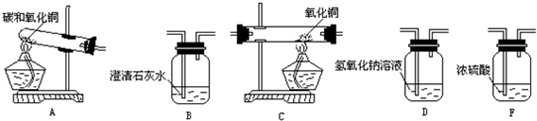
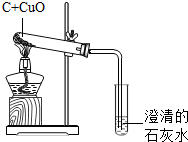 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:实验中观察到:黑色粉末变红色,澄清石灰水变浑浊.
小明根据上述现象认为:碳还原氧化铜可以生成铜和
提出疑问1:“碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
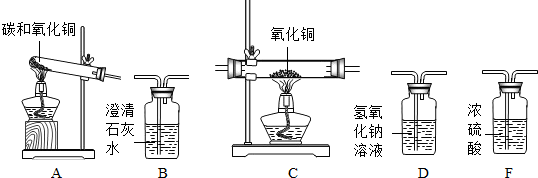
设计实验:小雨同学打算用下面的一些实验装置设计一套组合装置以检测碳还原氧化铜时生成的气体的成分.
若要证明碳还原氧化铜生成的气体中是否含有CO和CO2,上述装置的连接顺序是(装置可重复使用):A→
实验中根据什么现象可判断产生的气体中含CO?
反思:小明认为上述装置存在不完善之处,你认为装置还需如何改进?
提出疑问2:碳还原氧化铜得到的红色固体是否一定是铜?
查阅资料:①C也能将CuO还原为红色固体Cu2O(该物质的名称为
②Cu2O+H2SO4═Cu+CuSO4+H2O
猜想:(1)红色固体只是Cu;
(2)红色固体是
(3)红色固体是
实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体放入烧杯中,向其中加入足量的稀硫酸,充分反应后,静置 | 若无现象 | 证明红色固体是________ |
| 若______,______ | 证明红色固体中肯定含有 _____,可能含有_____ |
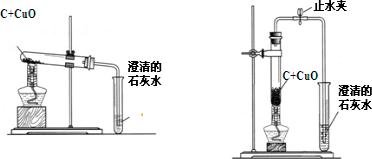

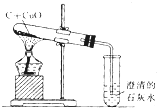 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下: