��Ŀ����
13�������Ҫ����գ���1��һ����̼�Ͷ�����ֻ̼��һ��֮�
�ٶ��߾��������ֵܣ�������ΪD������ĸ����
A�����Ƕ��ж� B��������ͬ�ַ��ӹ���
C�����Ƕ�������ˮ D��������ͬ��Ԫ�����
�ڶ���ѧ���������Զ�����һ��˵����������̼����ȼ�գ�һ����̼����ȼ�գ��������̼����ˮ��Ӧ��һ����̼���ܻ������̼����ʯ��ˮ��Ӧһ����̼���ܻ�һ����̼��������ͭ��Ӧ������̼���ܣ�����
��2�������������ж�����̼����������������Ҫԭ���ǻ�ʯȼ�ϵ�ȼ�գ�
��3������̼����һ���������Ҳ��һ������̬�ȣ��������������ϡ���̼��Ҫ�����AD
������ţ�
A���ᳫʹ��һ�������ϴ����� B�����������������������г�����
C������ֲ�����֣���ֹ�ҿ��ķ� D��Ϊ�˷��㣬�������ֹرյ�����Դ��
���� ��1������һ����̼�Ͷ�����̼�Ļ�ѧʽ������������ʣ����ж������ʵķ��ӹ��ɲ�ͬ�����Ԫ����ͬ�����������������ѧ���ʲ�ͬ��
һ����̼���п�ȼ�ԡ���ԭ�ԺͶ��ԣ���������̼�Ȳ�֧��ȼ��Ҳ����ȼ�ա�����ˮ��Ӧ����ʹ����ʯ��ˮ����ǣ������廯ѧ������غܴ�
��2��������̼���ŷ���Ҫ�Ӻ�̼���ʵ�ȼ�տ��ǣ�
��3������̼������ָ����������Ϣʱ�����õ�����Ҫ�������٣��ر��Ǽ��ٶ�����̼���ŷ�����������̬�����Դӽڵ硢���ܺͻ��յȻ������ı�����ϸ�ڣ��ݴ˽��з�����ɣ�
��� �⣺��1����һ����̼�Ļ�ѧʽΪCO��������̼��ѧʽΪCO2�������嶼����C��O����Ԫ����ɣ���������ķ��ӹ��ɲ�ͬ��CO������ˮ������ѪҺ��Ѫ�쵰��϶����ֳ����ԣ�CO2������ˮ���������D��
��һ����̼���п�ȼ�ԣ�������̼����ȼ�գ�һ����̼���л�ԭ�ԣ�������̼�ɱ��ֳ������ԣ�һ����̼���ж����壬������̼���ԣ�������̼����ˮ������ʯ��ˮ��Ӧ����һ����̼���ܣ����������̼����ȼ�գ�һ����̼����ȼ�գ��������̼����ˮ��Ӧ��һ����̼���ܻ������̼����ʯ��ˮ��Ӧһ����̼���ܻ�һ����̼��������ͭ��Ӧ������̼���ܣ���
��2����ʯȼ���к��д�����̼Ԫ�أ�������������ʯȼ�ϵ�ȼ�գ������˴����Ķ�����̼�������ʯȼ�ϵ�ȼ�գ�
��3����̼������Ǽ��ٶ�����̼���ŷţ���Ҫ�ӽ��ܡ��ڵ�ͽ��������濼�ǣ�A�������������ϴ�ʱ���ĵ���Դ���Ӷ������˶�����̼�ŷţ�B�ɼ�������ȼ�ϵ�ȼ�գ����ٶ�����̼�ŷţ�C������ǿֲ��Ĺ�����ã����������̼�����գ��Ӷ������˶�����̼���ŷţ�
���AD��
���� ������Ҫ����ѧ��������ѧ��ѧ֪ʶ�ۺϷ����ͽ��ʵ�������������������ѧ�����������˼ά��ȣ�ǿ����ѧ������֪ʶ��������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
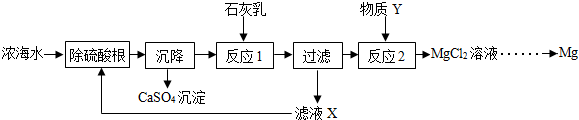
��1����ȫ�ɱ�������ʯ�������Ӧת���������������Ӧ�
����$\stackrel{����}{��}$��ʯ��$\stackrel{����}{��}$ʯ����
��2��д����Ӧ1�Ļ�ѧ����ʽ��Ca��OH��2+MgCl2=CaCl2+Mg��OH��2����
��3����ҺX�����ʵ���Ҫ�ɷ���CaCl2��NaCl���ѧʽ����
��4������Y�����������ᣮ
��5����MgCl2��Һ��һ�������������ᾧ�����ڵ����Ƶý���þ����2LŨ��ˮ�����Ͽɵõ�����þ������Ϊ57.6g��