题目内容
10.向含有氯化亚铁、氯化铜、氯化铝的溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生,下列推理合理的是( )| A. | 滤液中一定有氯化亚铁和氯化锌,可能含有氯化铜 | |
| B. | 滤液中一定有有氯化铜和氯化锌,可能含氯化亚铁 | |
| C. | 滤液中一定有氯化亚铁和氯化铜,可能含有氯化锌 | |
| D. | 滤渣中一定有铜和铁,可能含有锌 |
分析 本题可根据金属活动顺序及物质的化学性质,采用逐一验证法进行解答,也可正向理论推断.
首先从滤出的固体不能和盐酸反应可以对A、B两项进行判断;其次从金属活动顺序及题中给的信息“一定量的锌粉”进行判断.
解答 解:根据金属活动顺序表知锌比铁活泼,铁比铜活泼,所以加入锌粉,首先锌粉和氯化铜溶液反应,置换出单质铜,如果锌粉足量可以再继续和氯化亚铁反应置换出铁.“充分反应后过滤,向滤出的固体中滴加稀盐酸,气泡产生”说明有生成铁单质,溶液中的铜全部置换出来,可能有锌剩余.
A、因为有铁生成,所以滤液中不可能含有氯化铜,故A不正确.
B、因为有铁生成,所以滤液中不可能含有氯化铜,故B不正确.
C、因为有铁生成,所以滤液中不可能含有氯化铜,一定含有氯化锌,所以C不正确.
D、滤渣中一定有铜和铁,可能含有锌,故D正确.
故选D.
点评 本题主要考查了学生对金属活动顺序表的运用以及半定量(如一定量、过量、少量等)概念的理解和掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
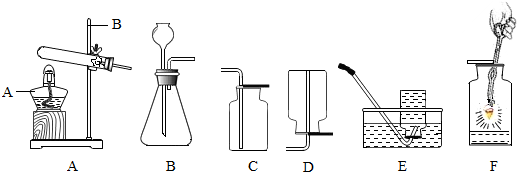
18.下列实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |

 请认真回忆物质与其构成粒子之间的关系,回答下列问题:
请认真回忆物质与其构成粒子之间的关系,回答下列问题: 保护水土资源人人有责,为了测定一定量黄河水中泥沙的质量,某同学设计了如图所示的实验操作:
保护水土资源人人有责,为了测定一定量黄河水中泥沙的质量,某同学设计了如图所示的实验操作: