题目内容
3.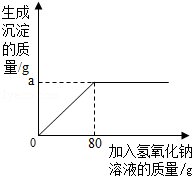 工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料提纯氯化镁;卤水中氯化镁的含量,需通过实验测得.检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系如图所示.
工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料提纯氯化镁;卤水中氯化镁的含量,需通过实验测得.检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系如图所示.(1)所得沉淀的化学式是Mg(OH)2;
(2)参加反应的氢氧化钠溶液中溶质的质量是16g;
(3)请计算卤水样品中氯化镁的质量分数.(写出计算过程)
分析 氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠;
根据氢氧化钠溶液质量、溶质质量分数可以计算氢氧化钠的质量;
根据氢氧化钠的质量可以计算氯化镁的质量,进一步可以计算卤水样品中氯化镁的质量分数.
解答 解:(1)沉淀是氢氧化镁,氢氧化镁的化学式是Mg(OH)2.
故填:Mg(OH)2.
(2)参加反应的氢氧化钠溶液中溶质的质量是:80g×20%=16g.
故填:16.
(3)设氯化镁的质量为x,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,
95 80
x 16g
$\frac{95}{x}=\frac{80}{16g}$
x=19g,
卤水样品中氯化镁的质量分数为:$\frac{19g}{100g}$×100%=19%,
答:卤水样品中氯化镁的质量分数为19%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
14.化学与生活息息相关.下列物质用途不合理的是( )
| A. | 干冰用作制冷剂 | B. | 医用酒精用于皮肤杀菌消毒 | ||
| C. | 小苏打用于治疗胃酸过多 | D. | 室内洒水防止煤气中毒 |
6.如图表示自来水消毒过程中发生反应的微观过程.下列叙述正确的是( )


| A. | 反应前后原子的种类和个数不变 | B. | 生成物中有三种不同的分子 | ||
| C. | 反应物中无单质 | D. | 反应前后元素化合价均无变化 |

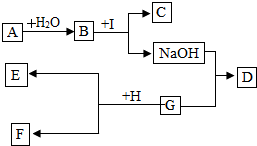 如图是初中化学中常见的物质之间的转换 关系,其中A为常用的食品干燥剂,C为白色沉淀,D 为蓝色沉淀,E为红色的固体单质.请你回答问题:
如图是初中化学中常见的物质之间的转换 关系,其中A为常用的食品干燥剂,C为白色沉淀,D 为蓝色沉淀,E为红色的固体单质.请你回答问题: