题目内容
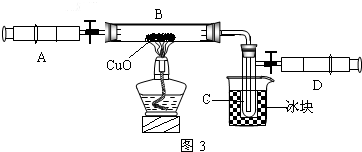
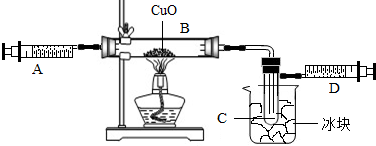
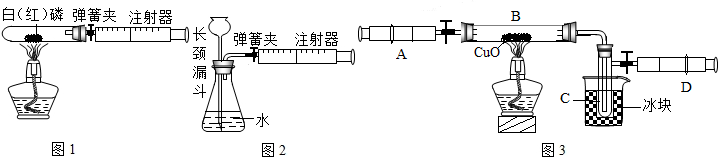
某学生为了测定由两种元素形成的气态化合物X的组成,做了如图所示的实验,把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应,得到如下结果:①实验前B管及药品的质量为21.3g,实验后为18.9g.
②C管中收集到的物质电解后可得到H2和O2,在D中收集到1.4gN2.

请回答下列问题:
(1)C中收集到的液体,质量是______g.
(2)在实验中看到的现象是______.
(3)X物质的相对分子质量是______.
(4)B中反应的化学方程式是______ 3Cu+3H2O+N2
【答案】分析:由实验前B管及药品的质量为21.3g,实验后为18.9g,C管中收集到的物质电解后可得到H2和O2,在D中收集到的是N2,我们可以得到X含有氮、氢两种元素.然后根据水中氢元素和氮气中氮元素的质量求出两元素的质量比进而可以确定X的化学式.
解答:解:(1)由题意 B管反应前后减少的质量为氧化铜中氧元素的质量,氧化铜中氧元素的质量和生成的水中氧元素的质量相等,即水中氧元素的质量=21.3g-18.9g=2.4g,所以水的质量=2.4g÷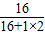 ×100%=2.7g;
×100%=2.7g;
(2)氧化铜与氨气反应生成铜和水和氮气.所以现象为黑色固体逐渐变为红色.C管中有无色液体出现;D的内管向外推动.
(3)我们可得X中含有氮、氧两种元素.其中氮元素和氢元素两元素的质量比是1.4g:(2.7g-2.4g)=14:3.所以我们可得氮、氧两种元素的原子个数比为1:3.所以化学式为NH3;相对分子质量=14+1×3=17;
(4)B中是氨气与氧化铜反应生成铜、氮气和水,其化学方程式为2NH3+3CuO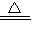 3Cu十N2+3H20.
3Cu十N2+3H20.
故答案为:(1)2.7;(2)黑色固体逐渐变为红色;C管中有无色液体出现;D的内管向外推动;
(3)17;(4)2NH3+3CuO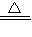 3Cu+3H2O+N2.
3Cu+3H2O+N2.
点评:装置B中氧化铜变为铜,所以减少的质量为氧化铜中氧元素的质量,而氧元素又与氨气中的氢元素接合成水,所以水中氧元素的质量与水中氧元素的质量相等.从而求出水的质量.
解答:解:(1)由题意 B管反应前后减少的质量为氧化铜中氧元素的质量,氧化铜中氧元素的质量和生成的水中氧元素的质量相等,即水中氧元素的质量=21.3g-18.9g=2.4g,所以水的质量=2.4g÷
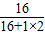 ×100%=2.7g;
×100%=2.7g;(2)氧化铜与氨气反应生成铜和水和氮气.所以现象为黑色固体逐渐变为红色.C管中有无色液体出现;D的内管向外推动.
(3)我们可得X中含有氮、氧两种元素.其中氮元素和氢元素两元素的质量比是1.4g:(2.7g-2.4g)=14:3.所以我们可得氮、氧两种元素的原子个数比为1:3.所以化学式为NH3;相对分子质量=14+1×3=17;
(4)B中是氨气与氧化铜反应生成铜、氮气和水,其化学方程式为2NH3+3CuO
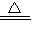 3Cu十N2+3H20.
3Cu十N2+3H20.故答案为:(1)2.7;(2)黑色固体逐渐变为红色;C管中有无色液体出现;D的内管向外推动;
(3)17;(4)2NH3+3CuO
 3Cu+3H2O+N2.
3Cu+3H2O+N2.点评:装置B中氧化铜变为铜,所以减少的质量为氧化铜中氧元素的质量,而氧元素又与氨气中的氢元素接合成水,所以水中氧元素的质量与水中氧元素的质量相等.从而求出水的质量.

练习册系列答案
相关题目