题目内容
17.现有一包固体粉末,可能由碳酸钠、硫酸钠、碳酸钙和氯化钠中的一种或几种组成,某同学想确定其组成成分,按如图所示步骤进行了如下实验(各步骤中加入的试剂均为足量):请回答:

固体粉末中肯定存在的物质是碳酸钠、硫酸钠(写化学式),用化学方程式表示白色沉淀部分溶解的原因BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
分析 根据碳酸钙难溶于水,碳酸根离子和钡离子会生成碳酸钡沉淀,硫酸根离子和钡离子会生成硫酸钡沉淀,碳酸钡沉淀会溶于酸,硫酸钡沉淀不溶于酸等知识进行分析.
解答 解:碳酸钙难溶于水,碳酸根离子和钡离子会生成碳酸钡沉淀,硫酸根离子和钡离子会生成硫酸钡沉淀,碳酸钡沉淀会溶于酸,硫酸钡沉淀不溶于酸.
取固体粉末加水搅拌充分溶解,得到澄清溶液,所以固体粉末中一定不含碳酸钙,加入氯化钡会生成白色沉淀,白色沉淀部分溶于硝酸,所以沉淀中含有碳酸钡和硫酸钡,固体粉末中一定含有硫酸钠、碳酸钠,固体粉末中是否含有氯化钠,不会影响题中的实验现象,所以固体粉末中可能含有氯化钠.
通过推导可知,固体粉末中肯定存在的物质是碳酸钠、硫酸钠,碳酸钡和硝酸反应生成硝酸钡、水和二氧化碳,所以白色沉淀部分溶解的化学方程式为:BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑;
故答案为:碳酸钠、硫酸钠;BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
点评 在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
6.化学实验是进行化学研究的重要方法.下列实验操作细节中,符合操作规范的是( )
| A. | 稀释浓硫酸时,将水倒入浓硫酸中,并用玻璃棒慢慢搅拌 | |
| B. | 为节约药品,将剩余的药品放回原瓶 | |
| C. | 加热蒸发皿内的溶液得到晶体时,等到溶液蒸干再停止加热 | |
| D. | 不慎碰倒酒精灯,桌上的酒精燃烧起来,立即用湿抹布盖灭 |


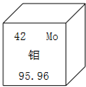 在元素周期表中钼元素的相关信息如图所示,下列说法正确的是C.
在元素周期表中钼元素的相关信息如图所示,下列说法正确的是C.