题目内容
8.氢氧化钾是一种重要的化工原料.将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主要成分是碳酸钾)在水中相互作用,也可生成氢氧化钾.(1)上述过程中发生反应的基本类型共有3种.
(2)发生复分解反应的化学方程式为Ca(OH)2+K2CO3=CaCO3↓+2KOH.
(3)如果要得到氢氧化钾溶液,还要经过过滤操作.
分析 本题是典型的文字叙述式信息给予题,根据创设的三个问题可知,要解决问题必须弄清制备氢氧化钾的反应过程,结合本题信息,再联想学过的氢氧化钠的制备,可以提炼出其中有效信息,明确其反应过程:①贝壳(主要成分是碳酸钙)灼烧:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;②灼烧后的固体与水作用:CaO+H2O═Ca(OH)2;③氢氧化钙与草木灰(主要成分是碳酸钾)在水中作用:Ca(OH)2+K2CO3═2KOH+CaCO3↓.以上三种反应就是三种基本类型,即分解反应、化合反应和复分解反应,要得到氢氧化钾溶液,需将CaCO3沉淀通过过滤操作除去.
解答 解:(1)贝壳(主要成分是碳酸钙)灼烧:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,属于分解反应,灼烧后的固体与水作用:CaO+H2O═Ca(OH)2,属于化合反应,氢氧化钙与草木灰(主要成分是碳酸钾)在水中作用:Ca(OH)2+K2CO3═2KOH+CaCO3↓,属于复分解反应,所以发生反应的基本类型共有3种;
(2)氢氧化钙与碳酸钾的反应为复分解反应,化学方程式为:Ca(OH)2+K2CO3=2KOH+CaCO3↓;
(3)要得到氢氧化钾溶液,需将CaCO3沉淀通过过滤操作除去.
故答案为:(1)3;
(2)Ca(OH)2+K2CO3=CaCO3↓+2KOH;
(3)过滤.
点评 本题为信息给予题,完成此题,可以根据题干提供的信息结合已有的氢氧化钠制取的知识进行.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
16.硫酸(H2SO4)是一种常见的酸,在硫酸中硫元素的化合价是( )
| A. | -2 | B. | +4 | C. | +6 | D. | 0 |
13.下列图示实验操作中,正确的是( )
| A. |  读液体体积 | B. |  称量固体质量 | C. |  过滤 | D. |  稀释浓硫酸 |
20. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应为化合反应 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中,乙、丁的质量变化之比为7:5 | |
| D. | 该反应中,甲、乙的质量变化之比为1:4 |
2. 乳酸分子结构如图所示,下列关于乳酸的叙述错误的是( )
乳酸分子结构如图所示,下列关于乳酸的叙述错误的是( )
 乳酸分子结构如图所示,下列关于乳酸的叙述错误的是( )
乳酸分子结构如图所示,下列关于乳酸的叙述错误的是( )| A. | 乳酸属于化合物 | |
| B. | 乳酸分子中碳、氢、氧的原子个数比为1:1:1 | |
| C. | 乳酸中氧元素的质量分数最大 | |
| D. | 乳酸由碳、氢、氧三种元素组成 |
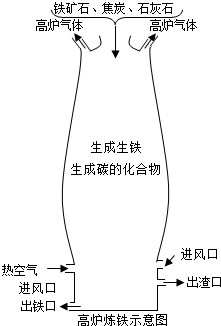 (1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.
(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.