题目内容
14.昊天同学探究氢氧化钠固体溶于水时其温度的变化后,由于疏忽,未将盛氢氧化钠固体试剂的瓶塞塞紧,一段时间后,它可能变质了.氢氧化钠变质的化学方程式为2NaOH+CO2=Na2CO3+H2O.昊天同学对该样品进行了系列探究:
【提出问题1】该样品真的变质了吗?
【实验方案1】取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,再向其中滴加氢氧化钙溶液,观察到生成白色沉淀说明样品真的变质了.
【提出问题2】该样品是部分变质还是全部变质?
【实验方案2】取该样品少量于烧杯里,加适量的水,搅拌,全部溶解后,再向其中加入过量的氯化钙溶液,产生白色沉淀,然后过滤,再向滤液里滴加无色酚酞试液,观察到变成红色,说明该样品是部分变质.发生反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl
【提出问题3】怎样除去样品中的杂质?
【实验方案3】将样品全部溶于水,向其中加入适量的氢氧化钙溶液,发生反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;然后过滤,再将滤液蒸干,即得到纯净的氢氧化钠固体.
分析 氢氧化钠变质后,含有杂质碳酸钠,检验氢氧化钠变质就是检验有碳酸根就行了,但在除杂时,所选择的药品只能跟杂质反应,不能跟主物质反应.同时也不能引进新的杂质.
解答 解:氢氧化钠吸收空气中的二氧化碳生成碳酸钠.因含有碳酸钠所以滴加氢氧化钙有白色沉淀生成.要检验是否含有氢氧化钠,加入的药品与碳酸钠反应不能生成氢氧化钠,故选用氯化钙溶液,而在除去碳酸钠时,所选的药品只能跟碳酸钠反应不能跟氢氧化钠反应,且不能引进新的杂质,故选用氢氧化钙溶液.
故答案为:
2NaOH+CO2=Na2CO3+H2O;
生成白色沉淀;
氯化钙;Na2CO3+CaCl2=CaCO3↓+2NaCl;
氢氧化钙;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
点评 检验是否含有碳酸钠和除去氢氧化钠中的碳酸钠是不一样.在除去杂质时,所选的药品只能跟杂质反应,不能跟主物质反应,且不能引进新的杂质.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
5.下列说法正确的是( )
| A. | 洗洁精和纯碱溶液都能清洗油污,其原理相同 | |
| B. | 焊锡的熔点比锡低,钢的硬度比铁大 | |
| C. | 用湿润的pH试纸测定某溶液的酸碱度,测定结果一定偏小 | |
| D. | 98.0%的浓硫酸与等质量水混合,得到49.0%的硫酸溶液 |
2.下列基本实验操作正确的是( )
| A. |  检查气密性 | B. |  测量溶液的pH | C. |  稀释浓硫酸 | D. |  加热固体 |
19.下列关于水的说法错误的是( )
| A. | 水是由氢气和氧气组成的 | B. | 水分子由氢原子和氧原子组成 | ||
| C. | 水由水分子构成 | D. | 水由氢气和氧气组成 |
17.小艳同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分5次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
试求:
(1)m的值为3.3.
(2)完全反应后最终所得溶液中溶质质量分数?(只求一种)(计算结果精确到0.1%)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀盐酸的质量g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量g | 1.1 | 2.2 | m | 4.4 | 4.4 |
(1)m的值为3.3.
(2)完全反应后最终所得溶液中溶质质量分数?(只求一种)(计算结果精确到0.1%)
18.实验操作有误或不规范,很可能造成实验失败或酿成事故.下列实验基本操作中正确的是( )
| A. |  闻气体气味 | B. | 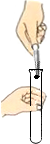 取用块状固体 | C. | 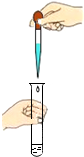 滴加液体 | D. | 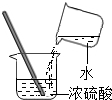 稀释浓硫酸 |
