题目内容
12.用20克氯酸钾与二氧化锰的混合物加热,到不再有气体产生后,残余固体质量为15.2克,问:(1)产生氧气的质量是多少克?
(2)原混合物中氯酸钾的质量分数是多少?
分析 (1)根据质量守恒定律可以计算出产生的氧气的质量;
(2)根据氧气的质量结合反应的化学方程式可以计算出氯酸钾的质量,进而可以计算出原混合物中氯酸钾的质量分数.
解答 解:(1)根据质量守恒定律可以得出氧气的质量为:20g-15.2=4.8g
(2)设原混合物中氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$
解得:x=12.25g
(2)原混合物中氯酸钾的质量分数是:$\frac{12.25g}{20g}$×100%=61.25%
答:(1)产生氧气的质量是4.8克;
(2)原混合物中氯酸钾的质量分数为61.25%.
点评 解答此类题的方法是:首先利用质量守恒定律,根据反应前后固体物质质量差求得反应生成气体的质量;然后,利用化学方程式由气体质量计算其他物质的质量.

练习册系列答案
相关题目
17.取6克石灰石,把40g稀盐酸分4次加入:
(1)6克石灰石中含杂质0.6克;
(2)m=2;
(3)样品中CaCO3的质量分数.
| 1 | 2 | 3 | 4 | |
| 加入盐酸质量 | 10 | 10 | 10 | 10 |
| 剩余固体质量 | 4 | m | 0.6 | 0.6 |
(2)m=2;
(3)样品中CaCO3的质量分数.
1.下列说法正确的是( )
| A. | 由一种元素组成的物质可能是纯净物 | |
| B. | 相对分子质量也是个比值 | |
| C. | 吸附一定是化学变化 | |
| D. | 一种元素在同一化合物中只有一种化合价 |
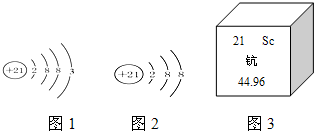
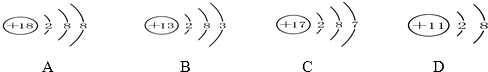

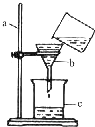 如图是某学生要完成的过滤操作,按要求完成题目
如图是某学生要完成的过滤操作,按要求完成题目