题目内容
一定质量的大理石与200g 18.25%的稀盐酸恰好完全反应,求:
(1)CO2的质量;
(2)反应后所得溶液中溶质质量分数.
(1)CO2的质量;
(2)反应后所得溶液中溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;由常见反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式计算出生成二氧化碳的质量、氯化钙的质量,进而可计算出反应后所得溶液中溶质质量分数.
解答:解:200g18.25%的稀盐酸中溶质的质量为200g×18.25%=36.5g.
设生成二氧化碳的质量为x,生成氯化钙的质量为y,参加反应的碳酸钙的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
z 36.5g y x
(1)
=
x=22g
(2)
=
y=55.5g
=
z=50g
反应后所得溶液中溶质质量分数为
×100%≈24.3%.
答:(1)CO2的质量为22g;(2)反应后所得溶液中溶质质量分数为24.3%.
设生成二氧化碳的质量为x,生成氯化钙的质量为y,参加反应的碳酸钙的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
z 36.5g y x
(1)
| 73 |
| 44 |
| 36.5g |
| x |
(2)
| 73 |
| 111 |
| 36.5g |
| y |
| 100 |
| 73 |
| z |
| 36.5g |
反应后所得溶液中溶质质量分数为
| 55.5g |
| 50g+200g-22g |
答:(1)CO2的质量为22g;(2)反应后所得溶液中溶质质量分数为24.3%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
铝热反应常用于冶炼或焊接金属,其反应原理可表示为3CuO+2Al═3Cu+Al2O3.现将一定量铝粉和氧化铜混合加热,充分反应后停止加热,为了检验氧化铜是否有剩余,取少量反应后的固体,加入足量稀硫酸,反应后将铁片插入上层溶液中.下列叙述的现象,能够说明氧化铜有剩余的是( )
| A、加热反应结束后有红色物质生成 |
| B、加入稀H2SO4后有气泡生成 |
| C、加入稀H2SO4后没有气泡生成 |
| D、插入溶液中的铁片表面有红色物质生成 |
日常生活中下列物质不属于盐的是( )
| A、调味的食盐 |
| B、透视用的钡餐BaSO4 |
| C、洗涤用的纯碱 |
| D、蔗糖 |
下列结构示意图所表示的粒子属于阳离子的是( )
A、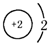 |
B、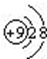 |
C、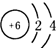 |
D、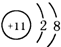 |
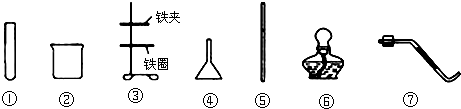
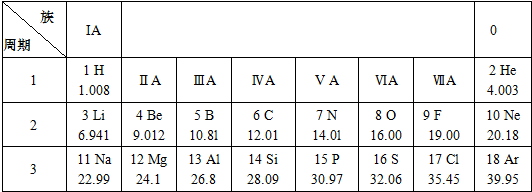
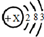 为某元素的原子结构示意图,该元素位于周期表中第
为某元素的原子结构示意图,该元素位于周期表中第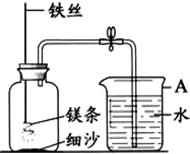 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.