题目内容
在元素周期表中,同一主族的元素化学性质相似,并且元素的性质有递变规律。请分析下表 属于同一主族的四种元素的有关信息,回答问题:

(1)请把上表中的空格补充完整。
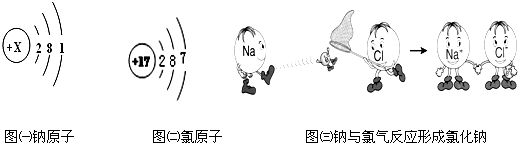
(2)①由原子结构示意图分析氟、氯、溴、碘化学性质相似的原因是:______;
②根据表格信息试归纳氟、氯、溴、碘对应单质与氢气的反应变化规律:___________ (答一点即可);
(3)已知Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的方程式为:HClO+NaOH=NaClO+H2O,写出Br2与氢氧化钠溶液反应的化学方程式:________。
(2)①由原子结构示意图分析氟、氯、溴、碘化学性质相似的原因是:______;
②根据表格信息试归纳氟、氯、溴、碘对应单质与氢气的反应变化规律:___________ (答一点即可);
(3)已知Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的方程式为:HClO+NaOH=NaClO+H2O,写出Br2与氢氧化钠溶液反应的化学方程式:________。
(1)
(2)①氟、氯、溴、碘原子的最外层电子数相同
②氟、氯、溴、碘单质与氢气反应的条件由易到难(或剧烈程度逐渐减弱等)
(3)Br2+2NaOH==NaBrO+NaBr+H2O

(2)①氟、氯、溴、碘原子的最外层电子数相同
②氟、氯、溴、碘单质与氢气反应的条件由易到难(或剧烈程度逐渐减弱等)
(3)Br2+2NaOH==NaBrO+NaBr+H2O

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目