题目内容
用2000 t Fe2O3质量分数为80%的赤铁矿,可炼出杂质质量分数为4%(杂质不含铁元素)的生铁多少吨?
解析:
|
可炼出杂质质量分数为4%的生铁1166.7 t. 解法1:设得到杂质质量分数为4%的生铁的质量为x. Fe2O3+3CO 160 112 2000 t×80% x·(1-4%) 解法2:因Fe2O3中的铁全部被还原成单质铁,故可利用铁元素守恒进行计算. 设可得杂质质量分数为4%的生铁的质量为x. 2000 t×80%× x=1166.7 t 解题指导:这是一道含杂质的计算题.化学方程式表示的是纯物质的质量关系,所以解题时应将不纯物质的质量换算成纯净物的质量才能代入方程式进行计算.这道题中给出的两个质量分数有本质的区别.80%对应的纯净物为Fe2O3,4%对应的是杂质.所以纯铁的质量应为生铁的质量×(1-4%),应将纯铁的质量代入化学方程式进行计算. |

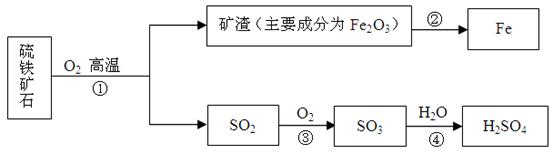
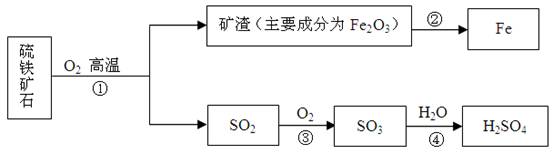
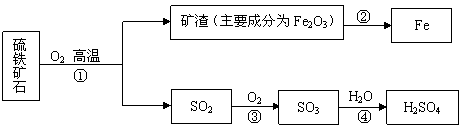
工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸。焙烧后的矿渣用于炼铁。其转化过程如下(部分条件和产物已略去)。
 |
请![]() 回答下列问题:
回答下列问题:
(1)上图出现的含硫元素的物质中,属于氧化物的有 (填化学式)。
(2)FeS2中的铁元素是+2价,硫元素的化合价为 。
(3)写出②处炼铁的化学方程式 。若用2000 t含杂质30%的矿渣炼铁,理论上可得到含铁98%的生铁质量为_________ t。
(4)在煤炭燃烧过程中也会产生SO2。工业上将煤燃烧产生的烟气通入吸收塔,用石灰水淋洗,外加氧气的作用,使之反应生成硫酸钙和水。请写出该反应的化学方程式 。