题目内容
下列化合物中,铁的质量分数最高的是( )
| A、FeO |
| B、Fe3O4 |
| C、Fe2O3 |
| D、FeCO3 |
考点:元素的质量分数计算
专题:化学式的计算
分析:根据化合物中元素的质量分数=
×100%,根据铁的化合物的化学式,通过变形使铁的原子个数相等,然后比较化合物中其它元素的原子的相对原子质量之和,其它原子的相对原子质量之和越小的,在该化合物中铁元素的质量分数就越大.
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:
在Fe3O4、Fe2O3、FeO、FeCO3四种物质中,将化学式变形得2Fe3O4、3Fe2O3、6FeO、6FeCO3,其它原子的相对原子质量之和越小的,因(12+16×3)×6>16×3×3>16×4×2>16×6,故在该化合物中铁元素的质量分数就越大,则铁元素的质量分数由大到小排列为FeO>Fe3O4>Fe2O3>FeCO3.
故选:A.
在Fe3O4、Fe2O3、FeO、FeCO3四种物质中,将化学式变形得2Fe3O4、3Fe2O3、6FeO、6FeCO3,其它原子的相对原子质量之和越小的,因(12+16×3)×6>16×3×3>16×4×2>16×6,故在该化合物中铁元素的质量分数就越大,则铁元素的质量分数由大到小排列为FeO>Fe3O4>Fe2O3>FeCO3.
故选:A.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
实验室用高锰酸钾制氧气时,不需要用到的仪器是( )
| A、量筒 | B、单孔橡皮塞 |
| C、酒精灯 | D、药匙 |
空气成分中用于制作霓虹灯的气体是( )
| A、二氧化碳 | B、稀有气体 |
| C、氧气 | D、氮气 |
根据已配平的反应式:铅丹+4HNO3═PbO2+2Pb(NO3)2+2H2O可以推测铅丹的化学式是( )
| A、Pb |
| B、PbO |
| C、PbO2 |
| D、Pb3O4 |
下列关于溶液颜色的说法正确的是( )
| A、氯化亚铁溶液是黄色的 |
| B、硫酸铜溶液是浅绿色的 |
| C、高锰酸钾溶液是紫红色的 |
| D、食盐水溶液是白色的 |
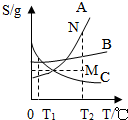 如图是物质A、B、C的溶解度曲线.下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线.下列相关说法正确的是( )| A、若要将B从溶液中结晶出来,常采用降温结晶的方法 |
| B、A的溶解度比B大 |
| C、T2℃时,组成在M点的A溶液为饱和溶液 |
| D、将T2℃时,C的饱和溶液降温至T1℃,则变为C的不饱和溶液(原溶液中无固体) |
已知氢气、一氧化碳、二氧化碳混合气体共20g,其中含碳元素质量为40%,将混合气体通入足量的氧化铜,再通入足量的石灰水,最后得到沉淀的质量可能是( )
| A、66.7g |
| B、30 g |
| C、100g |
| D、12 |
下列能由相应金属和酸直接反应得到的物质是( )
| A、AgCl |
| B、ZnSO4 |
| C、FeCl3 |
| D、CuSO4 |