题目内容
实验室常用铁和稀硫酸反应制取氢气,现用36g含有杂质的铁和足量的稀硫酸反应(杂质不与稀硫酸反应),共制得1g氢气,求铁的质量分数是多少?
解:设制取1g氢气需要铁的质量为x
Fe+H2SO4═FeSO4+H2↑
56 2
x 1g
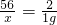
x=28g
铁的质量分数= ×100%=77.8%
×100%=77.8%
答:铁的质量分数为77.8%.
分析:根据反应的化学方程式可以表示反应中铁与放出氢气的质量关系,由实际产生氢气的质量计算不纯铁中所含铁的质量,求出铁的质量分数.
点评:本题主要考查学生利用化学方程进行计算的能力.学生要正确分析数量关系,找出有效数据进行计算,不要被其它数据干扰思维.
Fe+H2SO4═FeSO4+H2↑
56 2
x 1g
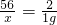
x=28g
铁的质量分数=
 ×100%=77.8%
×100%=77.8%答:铁的质量分数为77.8%.
分析:根据反应的化学方程式可以表示反应中铁与放出氢气的质量关系,由实际产生氢气的质量计算不纯铁中所含铁的质量,求出铁的质量分数.
点评:本题主要考查学生利用化学方程进行计算的能力.学生要正确分析数量关系,找出有效数据进行计算,不要被其它数据干扰思维.

练习册系列答案
相关题目
 如图是实验室制取气体常用的发生装置.用题中给出的方法制取各气体时,不能选用该发生装置的是( )
如图是实验室制取气体常用的发生装置.用题中给出的方法制取各气体时,不能选用该发生装置的是( )
