题目内容
小明同学在做盐酸和氢氧化钠的中和反应实验后,为判断反应后酸是否过量,下列方法不可取的是( )
| A、向反应后的溶液中滴加石蕊试液,观察溶液是否变红 |
| B、向反应后的溶液中加入碳酸钠,观察是否有气泡产生 |
| C、用pH试纸测反应后的溶液,看pH是否小于7 |
| D、向反应后的溶液中滴加硝酸银溶液,观察溶液中是否有沉淀产生 |
考点:中和反应及其应用,酸的化学性质
专题:常见的酸 酸的通性
分析:A、根据紫色石蕊在酸性溶液中变红色进行分析;
B、根据碳酸钠和酸反应会生成二氧化碳进行分析;
C、根据酸性溶液的pH值小于7进行分析;
D、根据氯离子会与银离子生成氯化银沉淀进行分析.
B、根据碳酸钠和酸反应会生成二氧化碳进行分析;
C、根据酸性溶液的pH值小于7进行分析;
D、根据氯离子会与银离子生成氯化银沉淀进行分析.
解答:解:A、取样品,滴入紫色石蕊,溶液变红,可以证明反应后酸过量,故A正确;
B、取样品,加入碳酸钠,碳酸钠和盐酸反应会生成二氧化碳气体,可以证明盐酸过量,故B正确;
C、酸性溶液的pH值小于7,用pH试纸可以判断盐酸过量,故C正确;
D、氯化钠中的氯离子也会与银离子生成氯化银沉淀,故D错误.
故选:D.
B、取样品,加入碳酸钠,碳酸钠和盐酸反应会生成二氧化碳气体,可以证明盐酸过量,故B正确;
C、酸性溶液的pH值小于7,用pH试纸可以判断盐酸过量,故C正确;
D、氯化钠中的氯离子也会与银离子生成氯化银沉淀,故D错误.
故选:D.
点评:本题主要考查了检验反应物的过量,需要依据反应物之间的不同离子,选择适当的物质,出现不同的现象即可鉴别.

练习册系列答案
相关题目
下列化学用语书写正确的是( )
| A、两个氧分子:2O | ||
| B、硫元素的化合价为负二价:S2- | ||
C、一个铝离子:
| ||
| D、三个一氧化碳分子:3CO |
下列关于空气成分的说法中不正确的是( )
| A、空气中的氧气主要来自植物的光合作用 |
| B、饼干在空气中变软是因为空气中含有水蒸气 |
| C、氮气的化学性质不活泼,可用于食品防腐 |
| D、稀有气体能做电光源,是因为其化学性质很不活泼 |
某溶液中含有Al3+、Mg2+、SO42--、NO3-四种离子,请根据选项判断,该溶液中Al3+、Mg2+、SO42-、NO3-的个数最简整数比依次可能是( )
| A、1:3:5:3 |
| B、1:3:2:2 |
| C、5:2:7:5 |
| D、1:2:3:4 |
下列物质变化中,其微观实质由分子分裂成原子,原子重新组合过程的是( )
| A、冰雪消融 | B、灯丝发光 |
| C、镁带燃烧 | D、玻璃破碎 |
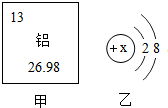 如图甲是由某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图:
如图甲是由某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图: