题目内容
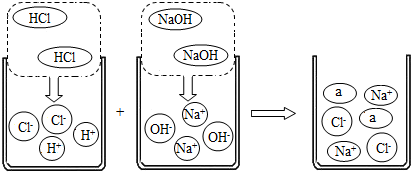
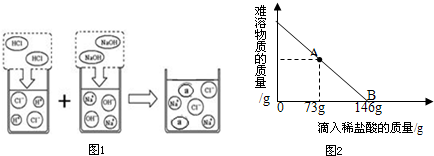
 图1表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化.请从图象中获取信息,回答下列问题:
图1表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化.请从图象中获取信息,回答下列问题:(1)如图2,进行该反应的实验操作是按照烧杯中以上
乙
乙
(填甲或乙)图所示进行,溶液的颜色变化是溶液由红色变为无色
溶液由红色变为无色
.(2)用溶质的质量分数为36.5%的盐酸40g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液的质量.
分析:(1)氢氧化钠溶液呈碱性,其pH大于7,盐酸呈酸性,其pH小于7,起始溶液的pH值大于7,所以可以判断是将稀盐酸滴入氢氧化钠溶液中,氢氧化钠溶液和盐酸恰好完全反应时溶液呈中性,而酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色,可以据此解答该题;
(2)根据反应的化学方程式结合盐酸的质量可以完成解答.
(2)根据反应的化学方程式结合盐酸的质量可以完成解答.
解答:解:(1)由图象可以看出,开始时溶液的pH大于7,呈碱性,表明是向氢氧化钠溶液中加入的盐酸,即按照烧杯中乙图所示进行的实验,酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色;
(2)溶质的质量分数为36.5%的盐酸40g含盐酸的质量为:40g×36.5%=14.6g
需要氢氧化钠溶液质量为x,
HCl+NaOH═NaCl+H2O
36.5 40
14.6g x
=
解得:x=16g
所以需要溶质的质量分数为20%的氢氧化钠溶液的质量为:16g÷20%=80g
答:需要溶质的质量分数为20%的氢氧化钠溶液的质量为80g
故答案为:(1)乙;溶液由红色变为无色;
(2)80g.
(2)溶质的质量分数为36.5%的盐酸40g含盐酸的质量为:40g×36.5%=14.6g
需要氢氧化钠溶液质量为x,
HCl+NaOH═NaCl+H2O
36.5 40
14.6g x
| 36.5 |
| 14.6g |
| 40 |
| x |
解得:x=16g
所以需要溶质的质量分数为20%的氢氧化钠溶液的质量为:16g÷20%=80g
答:需要溶质的质量分数为20%的氢氧化钠溶液的质量为80g
故答案为:(1)乙;溶液由红色变为无色;
(2)80g.
点评:本题以图象的形式考查了酸碱中和反应时溶液PH的变化,以及物质间的质量关系,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目




 (1)某化学兴趣小组的同学为了体验“工业冶炼金属”的过程.在实验室做了CO还原CuO的实验,他们称得装有CuO粉末的试管重102g,反应完全后,恢复到室温称量,试管和固体残留物共重100.4g,并收集到CO2 4.4g,请你和他们一起计算:
(1)某化学兴趣小组的同学为了体验“工业冶炼金属”的过程.在实验室做了CO还原CuO的实验,他们称得装有CuO粉末的试管重102g,反应完全后,恢复到室温称量,试管和固体残留物共重100.4g,并收集到CO2 4.4g,请你和他们一起计算: