题目内容
在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的pH变化如图所示.?
(1)该实验操作是将______溶液滴加到另一种溶液中.?
(2)图中M所对应溶液中所含溶质的化学式是______.
(1)该实验操作是将______溶液滴加到另一种溶液中.?
(2)图中M所对应溶液中所含溶质的化学式是______.

(1)由图示可知在没有加入该种试剂前,原溶液的pH值大于7,所以原来溶液显碱性,随着加入试剂,溶液的PH值减小,所以是将盐酸滴入氢氧化钠溶液中;
(2)因为氢氧化钠与盐酸反应生成氯化钠和水,所以反应后溶液中溶质有氯化钠;图中M点pH值小于7,说明盐酸过量,所以溶质中含有过量的氯化氢.
故答案为:(1)盐酸;(2)NaCl、HCl.
(2)因为氢氧化钠与盐酸反应生成氯化钠和水,所以反应后溶液中溶质有氯化钠;图中M点pH值小于7,说明盐酸过量,所以溶质中含有过量的氯化氢.
故答案为:(1)盐酸;(2)NaCl、HCl.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
小何进行盐酸和氢氧化钠中和反应的实验,在向烧杯中的氢氧化钠溶液滴加了一定量的稀盐酸后,才发现忘记了加入指示剂。为了判断该反应所得溶液的酸碱性,他进行了如下探究:
【提出问题】小何要探究的问题是 。
【猜想与假设】所得溶液可能显碱性,也可能显酸性,还可能显 性。
若溶液显碱性,则溶液中使其显碱性的离子是 (填写离子符号)。为避免碱性溶液污染环境,要对所得溶液进行沉淀处理,你认为处理的方法是 。
【实验与分析】小何从烧杯中取了部分反应后的溶液置于一试管中,并向试管中滴加了几滴无色酚酞试液,震荡,观察到试液不变色,于是他得出了溶液显中性的结论。小张认为小何得出的结论不正确,你认为小张的理由是 。
为了进一步确定溶液的酸碱性,小张取试管中的溶液做以下几个实验,你认为可行的是 (溶于水的二氧化碳忽略不计)。
| A.取样,滴加硫酸钠溶液,观察现象 |
| B.取样,加入锌粒.观察现象 |
| C.取样,通入二氧化碳,观察现象 |
| D.取样,滴加氢氧化钠溶液,观察现象 |
27.Ⅰ、在10%的硫酸溶液中存在着自由移动的微粒是______(填微粒符号),它能和l0%的氢氧化钠溶液发生______反应(填反应类型),反应过程中不断减少的微粒是______(填微粒符号).当两者恰好完全反应时,两种溶液中溶质的计量数之比等于______(用恰当的符号表示).
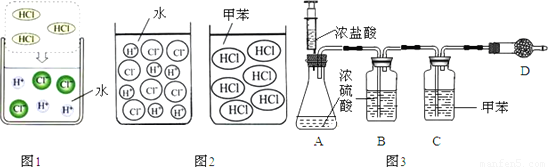
Ⅱ、盐酸是氯化氢(HCl)气体溶于水形成的溶液,HCl是极易溶于水的无色气体.图1为HCl气体溶于水的微观示意图.HCl气体也可溶于甲苯(一种有机溶剂),得氯化氢的甲苯溶液.
某化学兴趣小组的同学对氯化氢与盐酸的化学性质是否相同进行了探究,请你参与探究过程.
[提出问题]氯化氢气体与盐酸的化学性质是否相同?
[查阅资料]
①氯化氢气体是由氯化氢分子构成的;
②在盐酸中存在氢离子、氯离子和水分子;
③氯化氢的甲苯溶液中氯化氢以分子的形式存在.
盐酸与氯化氢的甲苯溶液的微观示意图2所示.
[分析猜想]氯化氢与盐酸的化学性质不一致.进行以上猜想的理由是:______.
[实验准备]为探究氯化氢与盐酸的化学性质,根据实验方案准备时发现缺少氯化氢的甲苯溶液.化学兴趣小组的同学向老师求助,老师用图3所示装置和有关试剂为兴趣小组制取了氯化氢的甲苯溶液.晴晴同学在协助老师制氯化氢的甲苯溶液时产生了疑问,请帮助解答.
(1)为什么浓盐酸加到浓硫酸中能产生大量的氯化氢气体?答:______.
(2)B装置中浓硫酸的作用是什么?答:______.
(3)D中装有用实验室常见的某种物质浓溶液浸湿的棉花,老师说其目的是除去尾气中的氯化氢,反应只生成盐和水.该物质是什么呢?答:______.
[进行实验]用盐酸和氯化氢的甲苯溶液进行对比实验.
[得出结论]盐酸与氯化氢气体的化学性质不一致.
Ⅱ、盐酸是氯化氢(HCl)气体溶于水形成的溶液,HCl是极易溶于水的无色气体.图1为HCl气体溶于水的微观示意图.HCl气体也可溶于甲苯(一种有机溶剂),得氯化氢的甲苯溶液.
某化学兴趣小组的同学对氯化氢与盐酸的化学性质是否相同进行了探究,请你参与探究过程.

[提出问题]氯化氢气体与盐酸的化学性质是否相同?
[查阅资料]
①氯化氢气体是由氯化氢分子构成的;
②在盐酸中存在氢离子、氯离子和水分子;
③氯化氢的甲苯溶液中氯化氢以分子的形式存在.
盐酸与氯化氢的甲苯溶液的微观示意图2所示.
[分析猜想]氯化氢与盐酸的化学性质不一致.进行以上猜想的理由是:______.
[实验准备]为探究氯化氢与盐酸的化学性质,根据实验方案准备时发现缺少氯化氢的甲苯溶液.化学兴趣小组的同学向老师求助,老师用图3所示装置和有关试剂为兴趣小组制取了氯化氢的甲苯溶液.晴晴同学在协助老师制氯化氢的甲苯溶液时产生了疑问,请帮助解答.
(1)为什么浓盐酸加到浓硫酸中能产生大量的氯化氢气体?答:______.
(2)B装置中浓硫酸的作用是什么?答:______.
(3)D中装有用实验室常见的某种物质浓溶液浸湿的棉花,老师说其目的是除去尾气中的氯化氢,反应只生成盐和水.该物质是什么呢?答:______.
[进行实验]用盐酸和氯化氢的甲苯溶液进行对比实验.
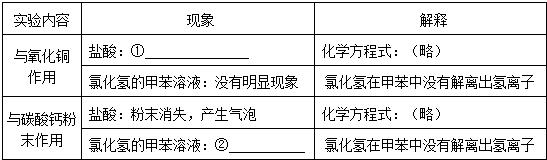
| 实验内容 | 现象 | 解释 |
| 与氧化铜作用 | 盐酸:① | 化学方程式:(略) |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢在甲苯中没有解离出氢离子 | |
| 与碳酸钙粉末作用 | 盐酸:粉末消失,产生气泡 | 化学方程式:(略) |
| 氯化氢的甲苯溶液:② | 氯化氢在甲苯中没有解离出氢离子 |