题目内容
某小组同学用下图所示的装置进行了两组兴趣实验(a、b管的体积相等,夹持装置已略去)。
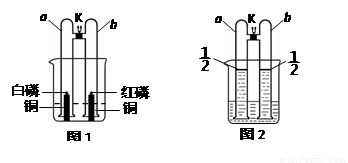
【资料】(1)白磷的着火点为40℃,红磷的着火点为240℃
(2)2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(1)如图1所示进行实验。关闭K,向烧杯中注入一定量的90℃的热水至图中虚线处。一段时间后,观察到a管中的现象是 。其中发生反应的化学方程式是 。对比a、b管中的实验现象,可得出燃烧的条件是 。
(2)如图2所示进行实验。关闭K,分别用排水集气法收集 体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。
【解析】(1)根据白磷着火点低,白磷燃烧产生白烟五氧化二磷,燃烧的条件进行解答
(2)根据镁和盐酸生成氯化镁和氢气,碳酸钙和盐酸生成氯化钙和水,二氧化碳,氢氧化钠和氯化钙生成氢氧化钙沉淀,二氧化碳和氢氧化钠反应时b管内压强减小,进行解答
【答案】
(1)白磷燃烧产生白烟,a管中液面上升 4P + 5O2 2P2O5
温度要达到可燃物的着火点
(2)Mg + 2HCl = MgCl2+ H2↑ a管内液面上升,b管内液面下降,最终相平,达到距管口约1/4 处。

练习册系列答案
相关题目
 (2010?北京)化学小组同学用下图所示装置(夹持仪器已略去)做了2个兴趣实验.每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出.
(2010?北京)化学小组同学用下图所示装置(夹持仪器已略去)做了2个兴趣实验.每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出.
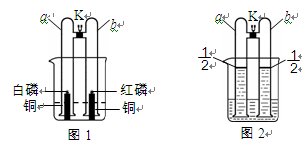
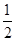 体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。
体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。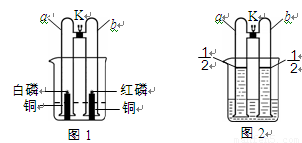
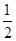 体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。
体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。