题目内容
10.在密闭的容器里,有A、B、C、D四种物质,在一定条件下反应,如图| A | B | C | D | |
| 反应前 | 10 | 2 | 10 | 10 |
| 反应后 | 4 | 待测 | 20 | 6 |
| A. | 物质C可能是单质 | B. | 物质B一定是催化剂 | ||
| C. | 该反应为分解反应 | D. | 物质A可能是单质 |
分析 根据已有的知识进行分析解答,在化学反应前后各物质的质量总和相等,根据反应物和生成物的种类确定反应的类型,据此解答.
解答 解:待测值为:10+2+10+10-4-20-6=2;
A、AD的质量反应后减少,故AD是反应物,C的质量反应后增加,故C是生成物,该反应是两种物质生成一种物质的化合反应,故C是化合物,错误;
B、B反应前后的质量不变,故B可能是反应的催化剂,错误;
C、该反应是化合反应,错误;
D、A是反应物,可能是单质,正确;
故选D.
点评 本题考查的是质量守恒定律的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20.下列说法正确的是( )
| A. | 分子是化学变化中的最小粒子 | |
| B. | 含有金属元素的离子一定是阳离子 | |
| C. | H和H+都属于氢元素,但它们的化学性质不同 | |
| D. | 盐的组成中一定含有金属元素 |
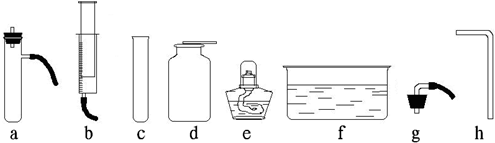
1.利用下列仪器进行实验(所有装置的气密性都已检查完毕)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有abdh(填字母).写出发生反应的文字表达式式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有产生氧气的速率均匀或可以得到平稳的氧气流等的优点.
(2)某同学继续探究“红砖粉末是否也可以作过氧化氢分解的催化剂?”实验步骤和现象如下:
①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
②将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
③用称量后的固体重复步骤①的实验,现象与步骤①完全相同.
试回答:步骤①中他除了选用试管外还用到上面列出的仪器有fgh(填字母).步骤③的实验目的是证明红砖粉末在反应前后的化学性质没有改变.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来实验开始没有称量红砖粉末的质量.可以用注射器代替的仪器是:胶头滴管和量筒
(3)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
(1)通过实验①和②对比可知,化学反应快慢与过氧化氢的浓度有关;
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有abdh(填字母).写出发生反应的文字表达式式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有产生氧气的速率均匀或可以得到平稳的氧气流等的优点.
(2)某同学继续探究“红砖粉末是否也可以作过氧化氢分解的催化剂?”实验步骤和现象如下:

①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
②将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
③用称量后的固体重复步骤①的实验,现象与步骤①完全相同.
试回答:步骤①中他除了选用试管外还用到上面列出的仪器有fgh(填字母).步骤③的实验目的是证明红砖粉末在反应前后的化学性质没有改变.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来实验开始没有称量红砖粉末的质量.可以用注射器代替的仪器是:胶头滴管和量筒
(3)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/0C | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)
15.下列有关实验现象的描述正确的是( )
| A. | 将试管内的适量水加热至沸腾:试管口有白烟产生 | |
| B. | 将块状的胆矾固体放在研钵内研碎:蓝色块状固体变成黑色粉末 | |
| C. | 硫酸铜溶液与氢氧化钠溶液反应:溶液中生成蓝色的沉淀 | |
| D. | 用小刀切下一小块石蜡,放入水中:固体逐渐消失 |
2.下列描述一定属于化学变化的是( )
| A. | 木柴能燃烧 | B. | 铁生锈 | C. | 爆炸 | D. | 发光放热的变化 |
20.下列符号中,能一个氧原子的是( )
| A. | O | B. | 2O | C. | 2O2 | D. | O2 |
 ,当x=10 时,其粒子符号为Ne.当x=8 时,其粒子符号为O2-,属阴离子.当x=11时,其粒子符号为Na+,属阳离子.
,当x=10 时,其粒子符号为Ne.当x=8 时,其粒子符号为O2-,属阴离子.当x=11时,其粒子符号为Na+,属阳离子.