题目内容
某化学学习小组的同学探究中和反应.
(1)甲同学向一定体积10%的氢氧化钠溶液中滴加10%的盐酸(常温下),测得反应中溶液的温度与加入盐酸体积的变化如下.
根据上表分析溶液温度变化的原因.
①加入盐酸的量在2~10 mL之间时________.
②加入盐酸的量在10~20 mL之间时________.
(2)乙同学用稀硫酸与氢氧化钠反应来探究中和反应的热量变化,进行了如下实验操作:取20%的稀H2SO4 30 mL,用温度计测量其温度为13℃.然后向其中加入5 g NaOH固体,充分反应后,测量其温度为22℃.
乙同学得出结论:稀H2SO4与NaOH固体反应放热.
①乙同学所得结论的依据是不严密的,原因:________.
②根据本实验目的,请你改进乙同学的实验操作,改进方案为:________.
(3)丙同学在做氢氧化钠与稀盐酸中和反应的实验时产生了疑问:在反应后的溶液中,氢氧化钠与稀盐酸是否恰好反应完全?请你帮助他设计实验进行探究.
![]()
答案:
解析:

解析:
(1)①随盐酸量的增加,中和反应放出的热量增大,溶液温度上升
②反应停止后,过量盐酸起冷却降温作用,热量散失
(2)①NaOH固体溶于水放出热量,温度升高并不能说明稀H2SO4与NaOH反应放出热量
②先将NaOH固体溶于水,冷却到室温13℃,然后再加入稀硫酸中,测其温度
(3)(答案合理即得分)


练习册系列答案
相关题目
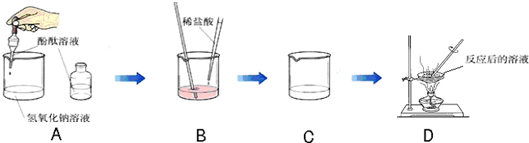
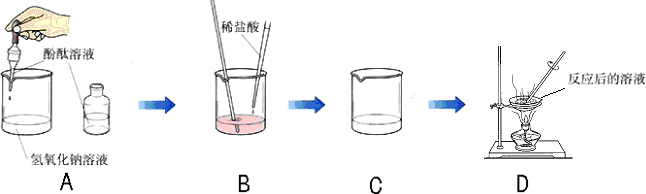
 实验是化学的灵魂,是学好化学的重要环节.
实验是化学的灵魂,是学好化学的重要环节.