��Ŀ����
��2006?�����һģ��ij��ѧѧϰС���ͬѧΪ��̽������������Һ��ϡ�����Ƿ�ǡ����ȫ��Ӧ����������ͼ��ʾ��ʵ�飺
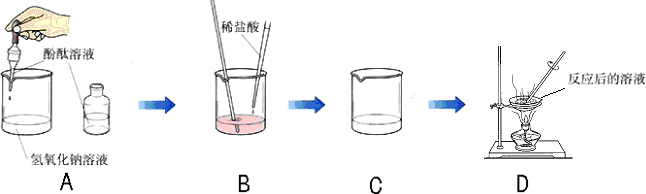
��1��ʵ���з�̪��Һ��������
��2��D����Һ���������µĹ����ǣ�д��ѧʽ��
��3��������ⶨ�������õ��Ĺ����к���CaCl2������ҺΪ���ԣ�����ôԭNaOH��Һ���ٶ����ᴿ�����п��ܻ��е������ǣ���дһ�����ʵĻ�ѧʽ��
ͬѧ��Ϊ�˳��Բⶨ����ʳ�Σ�������CaCl2���������������ᴿ����������ʵ�飮�����ʵ��ش��й����⣺
��ȷ��ȡ10g������Ʒ��������������ˮ�У��ټ������������ij��Һ����Ӧ����ˣ��ó�����1g�������ij��Һ��
A��NaOH B��K2CO3 C��Na2CO3 D��AgNO3 E��HCl��ϡ��
�䷴Ӧ�Ļ�ѧ����ʽ��
������Һ�м��������ϡ���ᣬ�������ϡ�����ԭ����
�۽�����ϡ��������Һ������������������������ȹ����У�Ҫ�ò��������Ͻ��裬��������
�ܼ�����Ʒ��NaCl����������Ϊ

��1��ʵ���з�̪��Һ��������
ָʾ���������������ʱǡ����ȫ��Ӧ��
ָʾ���������������ʱǡ����ȫ��Ӧ��
����2��D����Һ���������µĹ����ǣ�д��ѧʽ��
NaCl��
NaCl��
����˵���˽��۵�ʵ��������B�е���Һ�ɺ�ɫ�����ɫ��
B�е���Һ�ɺ�ɫ�����ɫ��
����3��������ⶨ�������õ��Ĺ����к���CaCl2������ҺΪ���ԣ�����ôԭNaOH��Һ���ٶ����ᴿ�����п��ܻ��е������ǣ���дһ�����ʵĻ�ѧʽ��
Ca��OH��2����CaCl2����
Ca��OH��2����CaCl2����
��ͬѧ��Ϊ�˳��Բⶨ����ʳ�Σ�������CaCl2���������������ᴿ����������ʵ�飮�����ʵ��ش��й����⣺
��ȷ��ȡ10g������Ʒ��������������ˮ�У��ټ������������ij��Һ����Ӧ����ˣ��ó�����1g�������ij��Һ��
C
C
�����ţ���A��NaOH B��K2CO3 C��Na2CO3 D��AgNO3 E��HCl��ϡ��
�䷴Ӧ�Ļ�ѧ����ʽ��
CaCl2+Na2CO3�TCaCO3��+2NaCl
CaCl2+Na2CO3�TCaCO3��+2NaCl
������Һ�м��������ϡ���ᣬ�������ϡ�����ԭ����
����Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
����Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
���۽�����ϡ��������Һ������������������������ȹ����У�Ҫ�ò��������Ͻ��裬��������
ʹҺ�����Ⱦ��ȣ���ֹҺ�ηɽ�
ʹҺ�����Ⱦ��ȣ���ֹҺ�ηɽ�
���ܼ�����Ʒ��NaCl����������Ϊ
88.9%
88.9%
����������1�����ݷ�ָ̪ʾ���ı�ɫ������
��2�������кͷ�Ӧ�IJ�����
��3��������������ƶϷ�Ӧ������ʳ��õķ����ǻ������ͳ��������������ɳ��� ������������Ȼ������������������Ȼ��Ƶ�����������
��2�������кͷ�Ӧ�IJ�����
��3��������������ƶϷ�Ӧ������ʳ��õķ����ǻ������ͳ��������������ɳ��� ������������Ȼ������������������Ȼ��Ƶ�����������
����⣺��1���������������ᷴӦû������������˼����̪��ͨ��ָʾ����ɫ�ı仯ָʾ�������������ᷴӦ���еij̶ȣ��ʴ�Ϊ��ָʾ���������������ʱǡ����ȫ��Ӧ��
��2���������������ᷴӦ�����Ȼ��ƺ�ˮ��D����Һ���������µĹ����� NaCl��B�е���Һ�ɺ�ɫ�����ɫ��˵���˽��ۣ�
��3���������õ��Ĺ����к���CaCl2������ҺΪ���ԣ�����ԭNaOH��Һ���ٶ����ᴿ�����п��ܻ��е�������
Ca��OH��2����CaCl2��������������ʱ�������ᷴӦ�����Ȼ��ƣ�
�ټ����ij��Һ�轫��Һ�еĸ�����ȫ��ת��Ϊ��������ѡC�䷴Ӧ�Ļ�ѧ����ʽ�� CaCl2+Na2CO3�TCaCO3��+2 NaCl
������Һ�м��������ϡ���ᣬ�������ϡ������Ϊ�� ����Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
�ۼ������������У�Ҫ�ò��������Ͻ��裬��ֹҺ�����Ȳ����ȣ�Һ�ηɽ���
�����Ȼ��Ƶ�����Ϊx��
CaCl2+Na2CO3=CaCO3��+2NaCl
111 100
x 1g
=
x=1.11g
�����Ȼ��Ƶ���������Ϊ
��100%=88.9%
�ʴ�Ϊ��
��1��ָʾ���������������ʱǡ����ȫ��Ӧ��
��2��NaCl��B�е���Һ�ɺ�ɫ�����ɫ��
��3��Ca��OH��2����CaCl2����
��C��CaCl2+Na2CO3�TCaCO3��+2 NaCl
�ڽ���Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
��ʹҺ�����Ⱦ��ȣ���ֹҺ�ηɽ�
��88.9%
��2���������������ᷴӦ�����Ȼ��ƺ�ˮ��D����Һ���������µĹ����� NaCl��B�е���Һ�ɺ�ɫ�����ɫ��˵���˽��ۣ�
��3���������õ��Ĺ����к���CaCl2������ҺΪ���ԣ�����ԭNaOH��Һ���ٶ����ᴿ�����п��ܻ��е�������
Ca��OH��2����CaCl2��������������ʱ�������ᷴӦ�����Ȼ��ƣ�
�ټ����ij��Һ�轫��Һ�еĸ�����ȫ��ת��Ϊ��������ѡC�䷴Ӧ�Ļ�ѧ����ʽ�� CaCl2+Na2CO3�TCaCO3��+2 NaCl
������Һ�м��������ϡ���ᣬ�������ϡ������Ϊ�� ����Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
�ۼ������������У�Ҫ�ò��������Ͻ��裬��ֹҺ�����Ȳ����ȣ�Һ�ηɽ���
�����Ȼ��Ƶ�����Ϊx��
CaCl2+Na2CO3=CaCO3��+2NaCl
111 100
x 1g
| 111 |
| x |
| 100 |
| 1g |
x=1.11g
�����Ȼ��Ƶ���������Ϊ
| 10g-1.11g |
| 10g |
�ʴ�Ϊ��
��1��ָʾ���������������ʱǡ����ȫ��Ӧ��
��2��NaCl��B�е���Һ�ɺ�ɫ�����ɫ��
��3��Ca��OH��2����CaCl2����
��C��CaCl2+Na2CO3�TCaCO3��+2 NaCl
�ڽ���Һ�й�����Na2CO3��ȫ��ȥ���Ա�������õ�������ʳ��
��ʹҺ�����Ⱦ��ȣ���ֹҺ�ηɽ�
��88.9%
�����������Լ����ᷴӦ���������������ָʾ����������ʱ������Լ�ֻ�������ʷ�Ӧ��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ