题目内容
现有10克铜锌合金,放入足量的稀硫酸中,充分反应后,测得产生的气体质量为0.2克,求:
(1)合金中铜的质量;
(2)合金中锌的纯度.
解:设合金中锌的质量为x,
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
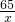 =
=
x=6.5g
(1)合金中铜的质量是:10g-6.5g=3.5g;
(2)合金中锌的纯度为: ×100%=65%.
×100%=65%.
答:合金中铜的质量是3.5g,合金中锌的纯度为65%.
分析:铜的金属活动性在(H)后,故铜不能与稀硫酸发生置换反应.因此,合金中只有锌和稀硫酸发生反应.根据反应的化学方程式和生成的氢气的质量,即可计算出合金中锌的质量.然后可求出铜的质量,并根据质量分数公式计算出锌的纯度.
点评:本题主要考查学生运用化学方程式和质量分数公式分析解答问题的能力,难度不大.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
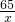 =
=
x=6.5g
(1)合金中铜的质量是:10g-6.5g=3.5g;
(2)合金中锌的纯度为:
 ×100%=65%.
×100%=65%.答:合金中铜的质量是3.5g,合金中锌的纯度为65%.
分析:铜的金属活动性在(H)后,故铜不能与稀硫酸发生置换反应.因此,合金中只有锌和稀硫酸发生反应.根据反应的化学方程式和生成的氢气的质量,即可计算出合金中锌的质量.然后可求出铜的质量,并根据质量分数公式计算出锌的纯度.
点评:本题主要考查学生运用化学方程式和质量分数公式分析解答问题的能力,难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
实验室中现有一种铜合金样品,已知此样品为铜锌合金、铜铝合金、铜银合金和铜铁合金中的一种,为确定其为四种合金中的哪一种,实验小组的同学们进行了下列的实验,请回答下列问题:
(1)实验室中有贴有如图所示标签的浓硫酸,要配制20%的稀硫酸350克,需该浓硫酸的体积是 mL;
(1)实验室中有贴有如图所示标签的浓硫酸,要配制20%的稀硫酸350克,需该浓硫酸的体积是
| 硫酸 体积:500mL 化学式:H2SO4 密度:1.4g/cm3 质量分数:50%(2)将20g合金粉末加入到98g新配好的稀硫酸中,恰好完全反应.过滤,将滤液蒸干后得到固体纯净物32.2g.通过计算回答: ①此合金为 ②写出发生反应的化学方程式: ③根据已知条件写出求解生成气体质量(x)的比例式: ④若向反应后所得滤液中加入89.4g水,则最终所得溶液中的溶质质量分数为 (3)若工业上用含Cu2S 70%的辉铜矿lOOt炼铜,并将其冶炼成上述铜的合金,(假设炼制过程中辉铜矿的损失率为10%),能炼出此铜合金的质量为 |
 某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.
某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.