题目内容
13.通过学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置.请结合下图回答问题:
(1)写出带标号的仪器的名称:a分液漏斗;b锥形瓶.
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性.
(3)实验室若用氯酸钾制取氧气,选择的发生装置是B;文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
实验室若用过氧化氢制取氧气,选择的发生装置是A.文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)a装置作用为便于添加液体试剂.
(5)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔.你认为制取乙炔应选择的发生装置是A;收集装置是C或E.
分析 (1)熟记仪器的名称;
(2)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(3)根据反应物的状态与反应条件确定制取装置,根据反应原理书写反应的文字表达式;
(4)根据仪器的用途来分析;
(4)乙炔制取属固液常温型制气,密度比空气略小,不溶于水的气体.
解答 解:(1)仪器a是分液漏斗,b是锥形瓶;故填:分液漏斗;锥形瓶;
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性.故填:检查装置的气密性;
(3)用氯酸钾制取氧气属于固体加热型,故选择装置B,氯酸钾在二氧化锰作催化剂加热的条件下分解为氯化钾和氧气;用过氧化氢制取氧气,属于固液常温型,所以选择装置A来制取,过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:B;氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;A;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(4)a是分液漏斗,便于添加液体试剂;故填:便于添加液体试剂;
(5)电石与水反应制取乙炔,固体与液体制取气体不需要加热,所以制取乙炔的发生装置选择B;密度比空气略小,不溶于水的气体,可用排水法收集.故填:A;C或E.
点评 发生装置的选择要看反应物的状态,固体与固体制取气体需加热,固体与液体制取气体不需要加热;收集装置的选择要看该气体的密度和溶解性,密度比空气大,用向上排空气法收集,密度比空气小,用向下排空气法收集,不易溶于水或难溶于水用排水法收集.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.漂白粉的主要成分为次氯酸钙[Ca(ClO)2],作漂白剂用于造纸、纺织工业.Ca(ClO)2中氯元素的化合价为( )
| A. | +2 | B. | +3 | C. | +1 | D. | -1 |
12.从微观角度对宏观现象作出解释,是化学学习的重要观点.下列解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 缉毒犬能根据气味发现毒品 | 分子在不断运动 |
| B | 用肉眼不能直接观察到二氧化碳分子 | 二氧化碳分子很小 |
| C | 冰受热变为水,水受热变为水蒸气 | 分子可以再分 |
| D | 固体碘受热升华 | 碘分子间的间隔增大 |
| A. | A | B. | B | C. | C | D. | D |
5.如图是硅元素在元素周期表中信息,下列有关硅元素说法不正确的是( )


| A. | 位于元素周期表的第三周期的中间 | B. | 原子核内质子数为14 | ||
| C. | 是地壳中最多的金属元素 | D. | 相对原子质量是28.09 |



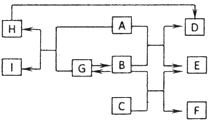 如图所示,A-I都是初中常见的物质,其中D是最清洁的能源,G和F都是红色固体,E和I含有元素的种类相同(箭头表示转化关系,部分反应物省略).回答下列问题
如图所示,A-I都是初中常见的物质,其中D是最清洁的能源,G和F都是红色固体,E和I含有元素的种类相同(箭头表示转化关系,部分反应物省略).回答下列问题