题目内容
正确的选择仪器和规范的实验操作是实验成功的保证.
(1)下列仪器中常用作少量药品反应容器的是______(填序号).
①量筒 ②漏斗 ③胶头滴管 ④试管 ⑤蒸发皿
(2)蒸发食盐水,用酒精灯加热的同时应______,以防液滴飞溅.
(3)欲用98%的浓硫酸,配制150g 10%的稀硫酸.量取所需水时,若俯视读数,则所配得的溶液溶质质量分数会______(填“偏大”或“偏小”).
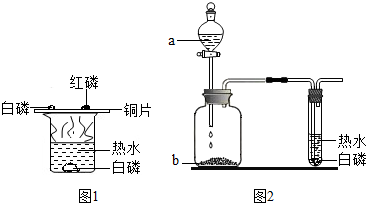
(4)某课外活动小组同学利用实验室仪器组装了下列两组装置做探究燃烧条件的兴趣实验.
如图1所示,能产生燃烧现象的是______(填字母):
A.水中的白磷
B.铜片上的白磷
C.铜片上的红磷
如图2所示,将液体a滴入瓶中并与固体b接触,能观察到白磷燃烧,则瓶内发生反应产生的气体是______.完成两组实验之后,同学们成功探究出燃烧所需要的三个条件:可燃物、氧气和______.
解:(1)试管常用作少量药品反应容器,故选④;
(2)蒸发食盐水,用酒精灯加热的同时应用玻璃棒不断搅拌,以防液滴飞溅,故答案为:用玻璃棒不断搅拌;
(3)俯视读数会导致所量取的液体实际体积小于所量值,即所量取的水的实际体积偏小,质量偏少,故所得溶液的质量分数偏大,故答案为:偏大;
(4)可燃物燃烧的条件是达到着火点,并与氧气接触,图1中铜片上的红磷不能燃烧,是因为温度不能达到它的着火点(240℃);水中的白磷不能燃烧,是因为不能与氧气接触;只有铜片上的白磷能够燃烧,因为即到达了着火点(40℃),又与氧气接触.故答案为:B;
热水中的白磷能够燃烧,说明生成的气体是氧气;燃烧所需要的三个条件:可燃物、与氧气接触和温度达到着火点,故答案为:氧气;温度达到着火点.
分析:(1)根据常用仪器的用途进行分析;
(2)根据蒸发食盐水的注意事项进行分析;
(3)量筒的读数正确的方法应该是视线与凹液面最低处相平,俯视读数会导致所量取的液体实际体积小于所量值,即所量取的水的实际体积偏小,质量偏少,故所得溶液的质量分数大于10%;
(4)根据燃烧的条件分析;根据白磷能够燃烧的现象分析反应生成的气体.
点评:量筒读数时视线与凹液面最低处相平,如果俯视仰均会导致读数值与实际值有较大的误差.做此类题一定要在稿纸上画出相应的图形,比较出读数值与实际所需液体体积之间的关系,进而分析结果.
(2)蒸发食盐水,用酒精灯加热的同时应用玻璃棒不断搅拌,以防液滴飞溅,故答案为:用玻璃棒不断搅拌;
(3)俯视读数会导致所量取的液体实际体积小于所量值,即所量取的水的实际体积偏小,质量偏少,故所得溶液的质量分数偏大,故答案为:偏大;
(4)可燃物燃烧的条件是达到着火点,并与氧气接触,图1中铜片上的红磷不能燃烧,是因为温度不能达到它的着火点(240℃);水中的白磷不能燃烧,是因为不能与氧气接触;只有铜片上的白磷能够燃烧,因为即到达了着火点(40℃),又与氧气接触.故答案为:B;
热水中的白磷能够燃烧,说明生成的气体是氧气;燃烧所需要的三个条件:可燃物、与氧气接触和温度达到着火点,故答案为:氧气;温度达到着火点.
分析:(1)根据常用仪器的用途进行分析;
(2)根据蒸发食盐水的注意事项进行分析;
(3)量筒的读数正确的方法应该是视线与凹液面最低处相平,俯视读数会导致所量取的液体实际体积小于所量值,即所量取的水的实际体积偏小,质量偏少,故所得溶液的质量分数大于10%;
(4)根据燃烧的条件分析;根据白磷能够燃烧的现象分析反应生成的气体.
点评:量筒读数时视线与凹液面最低处相平,如果俯视仰均会导致读数值与实际值有较大的误差.做此类题一定要在稿纸上画出相应的图形,比较出读数值与实际所需液体体积之间的关系,进而分析结果.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某课外活动小组的同学用下图所示装置,对氧化铜粉末(含铜粉)样品进行实验.图中铁架台等装置已略去.请回答有关问题:

(1)实验目的: .
(2)实验现象和有关化学方程式:
(3)实验数据记录和处理:
经过规范的操作和正确的称量,得到如下两组数据(IB中反应完全,C中吸收完全):
通过计算,同学们发现,用得到的两组数据求出的样品中氧化铜的质量分数不同.你觉得应该选择,哪组数据?请计算出样品中氧化铜的质量分数.
(4)问题和讨论:
经过讨论,同学们对装置进行了改进,在A与B之间增加了一个装置,再次实验后,用得到的两组数据求出的样品中氧化铜的质量分数基本相同.A与B之间增加的装置是(写出仪器名称和所盛药品) .

(1)实验目的:
(2)实验现象和有关化学方程式:
| 实验现象 | 化学方程式 | ||||
| A中反应产生大量气泡; | A中: | ||||
| B中黑色粉末逐渐变红色; | B中:CuO+H2
| ||||
| C中白色粉末逐渐变蓝色. | C中;CuS04+5H20═CuS04?5H20 |
经过规范的操作和正确的称量,得到如下两组数据(IB中反应完全,C中吸收完全):
| 反 应 前 | 氧化铜完全反应后 | |
| ①组 | B:玻璃管的质量30.8克 氧化铜样品的质量5.0克 |
B:玻璃管和管内固体物质的质量35.0克、 |
| ②组 | C:干燥管和硫酸铜的质量40.O克 | C:干燥管和管内固体物质的 质量41.0克 |
(4)问题和讨论:
经过讨论,同学们对装置进行了改进,在A与B之间增加了一个装置,再次实验后,用得到的两组数据求出的样品中氧化铜的质量分数基本相同.A与B之间增加的装置是(写出仪器名称和所盛药品)
(2004?金华)某课外活动小组的同学用下图所示装置,对氧化铜粉末(含铜粉)样品进行实验.图中铁架台等装置已略去.请回答有关问题:

(1)实验目的:______.
(2)实验现象和有关化学方程式:
(3)实验数据记录和处理:
经过规范的操作和正确的称量,得到如下两组数据(IB中反应完全,C中吸收完全):
通过计算,同学们发现,用得到的两组数据求出的样品中氧化铜的质量分数不同.你觉得应该选择,哪组数据?请计算出样品中氧化铜的质量分数.
(4)问题和讨论:
经过讨论,同学们对装置进行了改进,在A与B之间增加了一个装置,再次实验后,用得到的两组数据求出的样品中氧化铜的质量分数基本相同.A与B之间增加的装置是(写出仪器名称和所盛药品)______.

(1)实验目的:______.
(2)实验现象和有关化学方程式:
| 实验现象 | 化学方程式 |
| A中反应产生大量气泡; | A中:______. |
| B中黑色粉末逐渐变红色; | B中:CuO+H2 Cu+H2 Cu+H2 |
| C中白色粉末逐渐变蓝色. | C中;CuS04+5H20═CuS04?5H2 |
经过规范的操作和正确的称量,得到如下两组数据(IB中反应完全,C中吸收完全):
| 反 应 前 | 氧化铜完全反应后 | |
| ①组 | B:玻璃管的质量30.8克 氧化铜样品的质量5.0克 | B:玻璃管和管内固体物质的质量35.0克、 |
| ②组 | C:干燥管和硫酸铜的质量40.O克 | C:干燥管和管内固体物质的 质量41.0克 |
(4)问题和讨论:
经过讨论,同学们对装置进行了改进,在A与B之间增加了一个装置,再次实验后,用得到的两组数据求出的样品中氧化铜的质量分数基本相同.A与B之间增加的装置是(写出仪器名称和所盛药品)______.