题目内容
18.金属材料在生产和生活中有着广泛的应用.(1)铜、铁、铝出现的先后顺序与金属的活动性有密切关系.用两个实验能验证铜、铁、铝的金属活动性:①在硫酸铝溶液中插入铁丝;②Fe+CuSO4=Cu+FeSO4(用化学方程式表示).
(2)铝具有很好的抗腐蚀性能,原因是4Al+3O2═2Al2O3(用化学方程式表示).
(3)生活中铁制品容易锈蚀,请写出一条自行车链条防锈常用的方法在链条上涂油.
分析 (1)根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(3)根据铁生锈的原理进行分析.
解答 解:(1)在反应①中证明了铝比铁活泼,在反应②中需要验证铁比铜活泼,铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;
(2)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,反应的化学方程式为:4Al+3O2═2Al2O3.
(3)铁生锈实质是铁和氧气、水共同反应的结果,只要破坏其中任何一个条件,即可防锈,所以自行车链条防锈常用的方法:在链条上涂油.
故答案为:
(1)Fe+CuSO4=FeSO4+Cu(答案合理即可);(2)4Al+3O2=2Al2O3;
(3)在链条上涂油(答案合理即可).
点评 本题考查的是金属的有关性质和应用以及金属活动性顺序的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.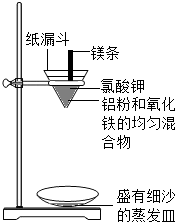 铝粉和氧化铁粉末在高温条件下能发生发应,该反应的实验装置如图,图中纸漏斗由两张滤纸折叠成漏斗状套在一起,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.同时还生成一种氧化物,冷却后熔融生成物能被磁铁吸引.
铝粉和氧化铁粉末在高温条件下能发生发应,该反应的实验装置如图,图中纸漏斗由两张滤纸折叠成漏斗状套在一起,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.同时还生成一种氧化物,冷却后熔融生成物能被磁铁吸引.
【查阅资料】铝粉和氧化铁粉末在高温条件下的反应叫铝热反应.实验中镁条和氯酸钾的作用是提供反应所需的高温条件.
请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
该反应属于的基本反应类型是置换反应.
该反应中单质铝与单质碳有相似的还原(填“氧化”或“还原”)性.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
某化学兴趣小组设计了如下实验方案并进行了探究.
【实验方案】(假设在该条件下,能发生反应的实验方案,反应完全进行)
【实验总结】通过上述实验探究.兴趣小组得出了金属与金属氧化物反应规律是位置在前的金属能将位于其后的金属从其金属氧化物中置换出来
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
 铝粉和氧化铁粉末在高温条件下能发生发应,该反应的实验装置如图,图中纸漏斗由两张滤纸折叠成漏斗状套在一起,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.同时还生成一种氧化物,冷却后熔融生成物能被磁铁吸引.
铝粉和氧化铁粉末在高温条件下能发生发应,该反应的实验装置如图,图中纸漏斗由两张滤纸折叠成漏斗状套在一起,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.同时还生成一种氧化物,冷却后熔融生成物能被磁铁吸引.【查阅资料】铝粉和氧化铁粉末在高温条件下的反应叫铝热反应.实验中镁条和氯酸钾的作用是提供反应所需的高温条件.
请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
该反应属于的基本反应类型是置换反应.
该反应中单质铝与单质碳有相似的还原(填“氧化”或“还原”)性.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
某化学兴趣小组设计了如下实验方案并进行了探究.
【实验方案】(假设在该条件下,能发生反应的实验方案,反应完全进行)
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 粉末呈红色. 固体部分溶解,有气泡产生,水溶液呈无色. | 镁能与氧化铜反应 |
| 实验2 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 粉末呈红色 固体部分溶解,有气泡产生,水溶液呈无色 | 锌能与氧化铜反应. |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 粉末呈红色 固体部分溶解,无气泡产生,水溶液呈黄色 | 铜不能与氧化铁反应. |
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
9.下列说法正确的是( )
| A. | 化石能源是可再生能源 | |
| B. | 二氧化碳是形成酸雨的主要原因 | |
| C. | 化肥不会造成任何污染 | |
| D. | PM10和PM2.5都是指空气中的污染颗粒物 |
6.下列实验操作中正确的是( )
| A. | 未经清洗的滴管再吸取其他试剂 | |
| B. | 实验剩余的药品放回原试剂瓶中 | |
| C. | 给试管内液体加热,试管口不要对着自己或他人 | |
| D. | 称量任何固体药品时,均要在天平的左右托盘上各放一张相同的纸片 |
13.1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,关于该物质的组成有下列论断,其中正确的是( )
①一定含C、H;②一定不含O;③可能含O;④一定含O;⑤分子中C、H的原子个数比为1:2;⑥分子中C、H的原子个数比为1:4.
①一定含C、H;②一定不含O;③可能含O;④一定含O;⑤分子中C、H的原子个数比为1:2;⑥分子中C、H的原子个数比为1:4.
| A. | ①②⑤ | B. | ①②⑥ | C. | ①③⑥ | D. | ①④⑤ |
3.草酸是“消字灵”的主要成分之一,分子结构如图.下列叙述不正确的是( )

| A. | 草酸的化学式为H2C2O4 | |
| B. | 草酸由2个氢原子、2个碳原子、4个氧原子构成 | |
| C. | 草酸中C、H两种元素的质量比为12:1 | |
| D. | 草酸中氧元素的质量分数最大 |