题目内容
诗词是民族灿烂文化的瑰宝.下列著名诗句中只含有物理变化的是( )
A. 野火烧不尽,春风吹又生
B. 粉身碎骨浑不怕,要留清白在人间
C. 夜来风雨声,花落知多少
D. 春蚕到死丝方尽,蜡炬成灰泪始干
C 【解析】试题分析∶诗词是民族灿烂文化的瑰宝。著名诗句中只含有物理变化的是C.夜来风雨声,花落知多少。 考点∶考查物理变化和化学变化的概念。 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案(1)下列实验现象描述正确的是____________(多选,用字母作答)
A.打开装有浓盐酸的试剂瓶,可看到白烟
B.湿润的有酚酞的滤纸靠近浓氨水,滤纸变红了
C.铁丝在氧气中剧烈燃烧生成了四氧化三铁
D.将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,液体显红色
E.向硫酸铜溶液中滴加氢氧化钠溶液有蓝色絮状沉淀
F.向氯化钙溶液中通入二氧化碳出现大量白色沉淀
(2)请从下列A,B两题中任选一个作答
A-测溶液的PH | B--酸碱中和反应 |
(1)先取少量待测液于______中(从所提供的仪器中选择合适序号) (2) 取待测液时用___________蘸取,滴在PH试纸上; (3)待测液滴在PH试纸上与标准比色卡比较PH=12,则该溶液呈______性。 | (1)先向氢氧化钠溶液中加入2-3滴无色酚酞,再用_______滴入稀盐酸;(从所提供的仪器中选择合适序号) (2)为了使酸和碱充分反应应该___________________(填操作方法) 。 (3)中和反应生成盐和_____(填化学式) |
可供选择仪器:A.漏斗 B.试管 C.量筒 D.蒸发皿 E..胶头滴管 |
在一次清洁厨房卫生时,小君发现厨房里某一铜制品表面出现了绿色,小君心里产生了疑问:这种绿色的物质由什么元素组成?为此,小君展开了探究。
【查阅资料】
①金属的锈蚀是一个缓慢氧化的过程。
②铁在有氧气和水等物质存在的条件下,发生复杂的化学反应,生成铁锈。
③空气中含有N2、O2、CO2、水蒸气等气体,在潮湿环境下,水蒸气的含量更多。
【猜想与假设】
①可能含氧元素
②可能含氢元素
③可能含有碳元素
④一定含有_______
⑤不可能含有氮元素
【实验与事实】
实验 | 操作 | 现象 | 结论 |
1 | 从铜器中取少量绿色物质于试管中,往试管里滴加稀盐酸。 | 观察到____________现象。 | 证明猜想①和③都成立。 |
观察到溶液由无色变成蓝绿色的现象。 | 证明猜想______成立。 | ||
2 | 从铜器中另取少量干燥的绿色物质于干燥的试管中,加热,观察试管口或者将产生的气体通过无水硫酸铜。 | 观察到试管口处有____现象或者观察到无水硫酸铜由白色变成_______色。 | 能同时证明猜想①和②都成立 |
【解释与结论】
铜器表面的绿色物质俗称铜绿,是由___________________________元素组成。
【拓展与交流】
①铜器表面要形成铜绿,需要与空气中的_________________________发生反应。
②上述实验2中加热后的试管中残留有黑色固体,后经证实是CuO ,CuO和二氧化锰一样,能够作为H2O2分解的催化剂,设计实验时,除了要探究CuO是否改变了H2O2分解反应速率,还要探究CuO的__________和___________是否改变。
铜元素 产生气泡 ④ 水雾生 蓝 铜、碳、氢、氧 氧气、水蒸气、二氧化碳 质量 化学性质 【解析】本题通过铜制品表面出现了绿色的情境,考查了碳酸根离子、水的检验,质量守恒定律,催化剂等。 猜想与假设:铜制品表面出现了绿色,绿色的物质中一定含有铜元素; 实验与事实:实验1:猜想①和③都成立,物质中可能含有碳酸根离子,含碳酸根离子物质与盐酸反应有气泡生成。从铜器中取少量绿色物质于试管...某些食品的包装袋内,放有装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”。某同学对一袋久置空气中的干燥剂进行了探究。
他先取部分久置干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液。然后对滤液的酸碱性和白色固体的组成作了探究。
(实验探究一)探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显____________性。
(实验探究二)探究过滤后白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3。
他查阅有关资料得知:CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量。氢氧化钙微溶于水。
(分析判断)你认为该过滤后得到的白色固体中一定不含有的物质是_______。
(实验操作)下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告。
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体,倒入适量水,充分搅拌、静置; ②向上层清液中滴加无色酚酞溶液 | 上层清液呈____色 | 白色固体中一定含有氢氧化钙 |
另取少量白色固体放入试管中,滴加稀盐酸 | _________ | 白色固体中一定含有碳酸钙 |
(总结反思)
只通过以上实验,还不能证明这袋久置于空气中的干燥剂中是否含有CaO。请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验:____。用化学方程式表示其中的反应_____。
(实验探究三)探究干燥剂样品中碳酸钙的质量分数
取上述干燥剂样品10g放入如图的装置中,充分反应后,测出了量筒中的水的体积为220mL,(此状况下二氧化碳的密度是2g/L),则此干燥剂中碳酸钙的质量分数为___________(通过计算填空)
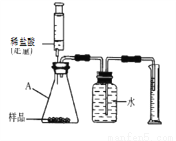
(总结反思)(实验探究三)中实验设计的不合理之处_________
碱性。 氧化钙或CaO 红 有气体产生 证明这袋干燥剂中含有较多量CaO的简易实验:取少量样品于试管中,加水溶解,触摸试管外壁,温度升高 CaO+H2O==Ca(OH)2 10% 生成的二氧化碳溶于水,与水发生反应,使二氧化碳的总体积减小 【解析】【实验探究一】如果久置的干燥剂中含有氧化钙,或含有氢氧化钙,或含有氧化钙和氢氧化钙,倒入适量水中,充分搅拌、过滤后的滤液中含有氢氧化钙,滤液显碱性...