题目内容
12.下列各组物质(每组的最后一种物质都是足量的),加适量水充分反应后,搅拌,过滤,滤纸上留下两种不溶性物质的一组是( )| A. | CaCl2,Ca(NO3)2,Na2CO3 | B. | MgSO4,Fe(OH)3,Ba(OH)2 | ||
| C. | Cu(NO3)2,HCl,NaOH | D. | Ag,Al,CuSO4 |
分析 根据物质的性质进行分析,酸碱盐之间要发生复分解反应,需符合复分解反应的条件,即反应有沉淀、或气体或水生成.位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:A、这三种物质相互间反应只能生成碳酸钙一种沉淀,错误;
B、这三种物质结合产生的沉淀有氢氧化镁、硫酸钡和氢氧化铁三种沉淀,错误;
C、这三种物质结合只能生成氢氧化铜一种沉淀,错误;
D、这三种物质结合,铝能置换出铜,银不反应,故沉淀是两种,正确;
故选D.
点评 本题考查了常见物质间的反应,完成此题,可以依据物质的性质进行,要求同学们熟记常见物质的水溶性,以便灵活应用.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
2.(多选)现有H2和O2的混合气体20g,点燃充分反应后恢复到常温剩下2g气体.原混合气体中H2和O2的质量比可能为( )
| A. | 1:4 | B. | 1:5 | C. | 1:8 | D. | 1:9 |
20.对浓硫酸进行稀释时,一定会用到的一组仪器是( )
| A. | 托盘天平、药匙 | B. | 烧杯、玻璃棒 | C. | 镊子、量筒 | D. | 水槽、试管 |
7.化学教师为了调动同学们探究的积极性,布置了一个探究任务:请同学们通过实验探究某企业采用的氨碱法制的纯碱样品的成分.
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
猜想一:只含有Na2CO3
猜想二:含有Na2CO3和NaHCO3
【查阅资料】
【实验探究】为了确定纯碱样品的成分,同学们设计如下实验方案,请你一起完成下列实验报告.
【实验反思】
实验步骤①中,加入氯化钙溶液过量的目的是将碳酸钠全部除去.
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
猜想一:只含有Na2CO3
猜想二:含有Na2CO3和NaHCO3
【查阅资料】
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 产生气泡 | 产生气泡 |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的氯化钙溶液. | 有白色沉淀产生 | 该反应的方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液滴加稀盐酸 | 有气泡冒出 | 该反应的方程式: Na2CO3+2HCl═2NaCl+H2O+CO2↑ 证明猜想②成立. |
实验步骤①中,加入氯化钙溶液过量的目的是将碳酸钠全部除去.
1.下列对实验现象的描述中,正确的是( )
| A. | 磷在氧气中燃烧,产生大量白雾 | B. | 木炭在空气中燃烧发出白光 | ||
| C. | 铁丝在氧气中燃烧火焰呈蓝色 | D. | 硫在氧气中燃烧发出蓝紫色火焰 |

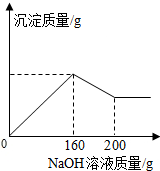 已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有稀硫酸、硫酸镁、硝酸钾、硫酸亚铁、氯化铝、碳酸钾中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列有关的判断正确的个数是( )
已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有稀硫酸、硫酸镁、硝酸钾、硫酸亚铁、氯化铝、碳酸钾中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列有关的判断正确的个数是( )