题目内容
27、如甲图所示,小明同学进行酸碱中和反应的实验,反应后为确定盐酸与氢氧化钠是否恰好完全反应,小明从烧杯中取少量反应后的溶液于一试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和的结论.
(1)小华认为小明的结论不正确,他认为除了“恰好完全中和”外还有第二种可能性,这种可能性是
(2)请你另设计一个实验,研究上述烧杯中的溶液是否恰好完全中和,填写下表:
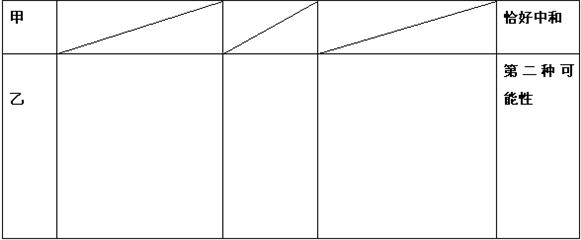
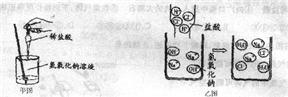
上面乙图是将盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图,请你回答:
(3)写出该反应的化学方程式:
(4)从图中可看出该反应的微观实质是

(1)小华认为小明的结论不正确,他认为除了“恰好完全中和”外还有第二种可能性,这种可能性是
盐酸过量
.(2)请你另设计一个实验,研究上述烧杯中的溶液是否恰好完全中和,填写下表:

上面乙图是将盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图,请你回答:
(3)写出该反应的化学方程式:
NaOH+HCl=NaCl+H2O
,该反应的基本反应类型是
复分解反应
.(4)从图中可看出该反应的微观实质是
H++OH-=H2O
.分析:酚酞在酸性和中性溶液中均为无色,仅仅根据酚酞为无色不能确定氢氧化钠和盐酸恰好完全反应,可以通过测反应后而要的PH的方法进行确定,氢氧化钠和盐酸反应生成氯化钠和水,此反应属于复分解反应,酸碱中和的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子.
解答:解(1)酚酞在酸性和中性溶液中均为无色,根据酚酞为无色说明溶液可能呈中性也可能呈酸性,所以本题答案为:盐酸过量;
(2)要想知道反应是否恰好进行,可以通过测反应后溶液的PH的方法,所以本题答案为:用玻璃棒蘸取反应后的溶液滴在PH试纸上,与标准比色卡对照,发现其PH小于7,说明溶液呈酸性,盐酸过量;
(3)氢氧化钠溶液和盐酸反应生成氯化钠和水,此反应为复分解反应,所以本题答案为:NaOH+HCl=NaCl+H2O,复分解反应;
(4)氢氧化钠和盐酸的反应为中和反应,中和反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子,所以本题答案为:H++OH-=H2O.
(2)要想知道反应是否恰好进行,可以通过测反应后溶液的PH的方法,所以本题答案为:用玻璃棒蘸取反应后的溶液滴在PH试纸上,与标准比色卡对照,发现其PH小于7,说明溶液呈酸性,盐酸过量;
(3)氢氧化钠溶液和盐酸反应生成氯化钠和水,此反应为复分解反应,所以本题答案为:NaOH+HCl=NaCl+H2O,复分解反应;
(4)氢氧化钠和盐酸的反应为中和反应,中和反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子,所以本题答案为:H++OH-=H2O.
点评:本题考查了酸碱中和反应的实质以及设计实验证明两者是否恰好完全反应,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如甲图所示,小明同学进行酸碱中和反应的实验,反应后为确定盐酸与氢氧化钠是否恰好完全反应,小明从烧杯中取少量反应后的溶液于一试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和的结论.
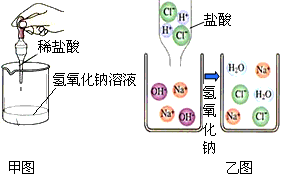
(1)小华认为小明的结论不正确,他认为除了“恰好完全中和”外还有第二种可能性,这种可能性是________.
(2)请你另设计一个实验,研究上述烧杯中的溶液是否恰好完全中和,填写下表:
| 甲 | / | / | / | 恰好中和 |
| 乙 | 第二种可能性 |
(3)写出该反应的化学方程式:________,该反应的基本反应类型是________.
(4)从图中可看出该反应的微观实质是________.
(2008?沂源县一模)如甲图所示,小明同学进行酸碱中和反应的实验,反应后为确定盐酸与氢氧化钠是否恰好完全反应,小明从烧杯中取少量反应后的溶液于一试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和的结论.
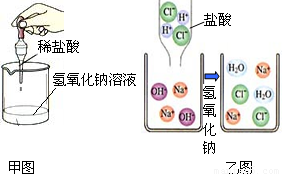
(1)小华认为小明的结论不正确,他认为除了“恰好完全中和”外还有第二种可能性,这种可能性是______.
(2)请你另设计一个实验,研究上述烧杯中的溶液是否恰好完全中和,填写下表:
上面乙图是将盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图,请你回答:
(3)写出该反应的化学方程式:______,该反应的基本反应类型是______.
(4)从图中可看出该反应的微观实质是______.

(1)小华认为小明的结论不正确,他认为除了“恰好完全中和”外还有第二种可能性,这种可能性是______.
(2)请你另设计一个实验,研究上述烧杯中的溶液是否恰好完全中和,填写下表:
| 甲 | / | / | / | 恰好中和 |
| 乙 | 第二种可能性 |
(3)写出该反应的化学方程式:______,该反应的基本反应类型是______.
(4)从图中可看出该反应的微观实质是______.
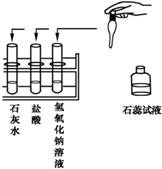 25、王老师在化学课上经常组织同学们开展一些探究活动:
25、王老师在化学课上经常组织同学们开展一些探究活动:
 化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.
化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.