题目内容
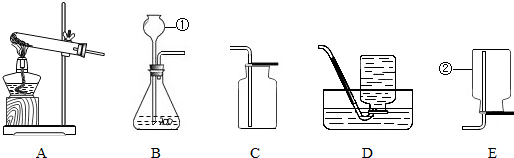
如图1是某兴趣小组同学在实验室里制取二氧化碳气体的装置图,请根据图来回答.

(1)该实验选用的固体试剂是 ,液体试剂是 .
(2)实验开始之前应先 .
(3)容器B中的导管口的位置在 处(填“c”或“d”).
(4)此实验中采用分液漏斗的优点是 ,
我们也可以将分液漏斗改为 ,此时加入A容器中的液体液面应到 处(根据图选填“a”或“b”).
(5)A装置还可用于制取的气体是 ,反应原理是 (用文字表达式表示).
(6)另一小组的同学为探究CO2的某一种性质,进行如图2的实验:
沉在大烧杯底部的红色气球充满空气,蓝色气球充满二氧化碳,将一集气瓶中的二氧化碳倾入大烧杯中,发现其中一只气球浮了起来,用手轻轻按压该气球,手一松气球又上浮.
请分析回答: 色气球浮起来,由此得出二氧化碳的这一性质是 ;如果继续向大烧杯中倾倒二氧化碳,另一只气球能出现与前一只气球同样的现象吗? .

(1)该实验选用的固体试剂是
(2)实验开始之前应先
(3)容器B中的导管口的位置在
(4)此实验中采用分液漏斗的优点是
我们也可以将分液漏斗改为
(5)A装置还可用于制取的气体是
(6)另一小组的同学为探究CO2的某一种性质,进行如图2的实验:
沉在大烧杯底部的红色气球充满空气,蓝色气球充满二氧化碳,将一集气瓶中的二氧化碳倾入大烧杯中,发现其中一只气球浮了起来,用手轻轻按压该气球,手一松气球又上浮.
请分析回答:
考点:二氧化碳的实验室制法,二氧化碳的物理性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:实验开始之前应先:检查装置的气密性;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.用分液漏斗的优点是:可以控制反应的速度;将分液漏斗改为长颈漏斗时,长颈漏斗的下端应该在液面以下;由题目的信息可知:红色气球浮起来,由此得出二氧化碳的这一性质是:二氧化碳的密度比空气的密度大;如果继续向大烧杯中倾倒二氧化碳,另一只气球不会上浮.因外界二氧化碳的密度与气球内二氧化碳的密度相同.
解答:解:(1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,故答案为:大理石或石灰石;稀盐酸;
(2)实验开始之前应先:检查装置的气密性,故答案为:检查装置的气密性
(3)用向上排空气法收集二氧化碳时,导管应该进入集气瓶的底部,故答案为:c
(4)用分液漏斗的优点是:可以控制反应的速度;将分液漏斗改为长颈漏斗时,长颈漏斗的下端应该在液面以下;故答案为:可以控制反应的速度;长颈漏斗;a;
(5)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,故答案为:氧气;过氧化氢
水+氧气;
(6)由题目的信息可知:红色气球浮起来,由此得出二氧化碳的这一性质是:二氧化碳的密度比空气的密度大;如果继续向大烧杯中倾倒二氧化碳,另一只气球不会上浮.因外界二氧化碳的密度与气球内二氧化碳的密度相同;故答案为:红;二氧化碳的密度比空气的密度大;另一只气球不会上浮.因外界二氧化碳的密度与气球内二氧化碳密度相同;
(2)实验开始之前应先:检查装置的气密性,故答案为:检查装置的气密性
(3)用向上排空气法收集二氧化碳时,导管应该进入集气瓶的底部,故答案为:c
(4)用分液漏斗的优点是:可以控制反应的速度;将分液漏斗改为长颈漏斗时,长颈漏斗的下端应该在液面以下;故答案为:可以控制反应的速度;长颈漏斗;a;
(5)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,故答案为:氧气;过氧化氢
| 二氧化锰 |
(6)由题目的信息可知:红色气球浮起来,由此得出二氧化碳的这一性质是:二氧化碳的密度比空气的密度大;如果继续向大烧杯中倾倒二氧化碳,另一只气球不会上浮.因外界二氧化碳的密度与气球内二氧化碳的密度相同;故答案为:红;二氧化碳的密度比空气的密度大;另一只气球不会上浮.因外界二氧化碳的密度与气球内二氧化碳密度相同;
点评:本考点主要考查了检查装置的气密性、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和二氧化碳的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目


 (1)根据下列要求用恰当的数字和符号表示
(1)根据下列要求用恰当的数字和符号表示 如图是A、B、C三种物质的溶解度曲线.根据图象回答:
如图是A、B、C三种物质的溶解度曲线.根据图象回答: