题目内容
学习了物质之间的相互转化关系后小明同学对用H2SO4、Fe和CuO来制取Cu设计了两套方案(如下),但是小明同学并未将方案写完整,请你将小明同学的方案补充完整.
方案一 ① ; ②Fe+CuSO4═FeSO4+Cu
方案二 ①Fe+H2SO4═FeSO4+H2↑; ②
看了方案后,老师给小明指出方案一有很多优点,如操作比较简单、制取过程安全,那么你能否再写出方案一的一条优点: .
方案一 ①
方案二 ①Fe+H2SO4═FeSO4+H2↑; ②
看了方案后,老师给小明指出方案一有很多优点,如操作比较简单、制取过程安全,那么你能否再写出方案一的一条优点:
考点:化学实验方案设计与评价,金属的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:简单实验方案的设计与评价
分析:根据获取铜的方法进行分析,可以使用活泼金属与铜盐溶液反应的方法获取铜,也可以使用氢气还原氧化铜的方法获取铜.
解答:解:(1)
方案一:①氧化铜与硫酸反应生成硫酸铜和水.该反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
②硫酸铜与铁反应生成硫酸亚铁和铜.该反应的化学方程式为:CuSO4+Fe═FeSO4+Cu.
方案二:
①铁与硫酸反应生成硫酸亚铁和氢气.该反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
②氢气与氧化铜在加热条件下反应生成铜和水.该反应的化学方程式为:H2+CuO
Cu+H2O.
(2)用氢气还原氧化铜时,需要加热,氢气与空气混合达到一定程度时,遇明火会发生爆炸,用方案二方法制取铜时,既需要加热,又不安全;
用方案一方法制取铜时,既不需要加热,又安全;用方案一方法制取铜时,需要的仪器比用方案二方法制取铜时需要的仪器少,并且操作比较简单.
故以上两个方案中,最好的是方案一,选择方案一的理由是:①节约能源(不需加热),②操作安全简便.
故答案为:
方案一①H2SO4+CuO=CuSO4+H2O; 方案二②H2+CuO=Cu+H2O
一条优点:可节约能源,可少浪费一些资源
方案一:①氧化铜与硫酸反应生成硫酸铜和水.该反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
②硫酸铜与铁反应生成硫酸亚铁和铜.该反应的化学方程式为:CuSO4+Fe═FeSO4+Cu.
方案二:
①铁与硫酸反应生成硫酸亚铁和氢气.该反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
②氢气与氧化铜在加热条件下反应生成铜和水.该反应的化学方程式为:H2+CuO
| ||
(2)用氢气还原氧化铜时,需要加热,氢气与空气混合达到一定程度时,遇明火会发生爆炸,用方案二方法制取铜时,既需要加热,又不安全;
用方案一方法制取铜时,既不需要加热,又安全;用方案一方法制取铜时,需要的仪器比用方案二方法制取铜时需要的仪器少,并且操作比较简单.
故以上两个方案中,最好的是方案一,选择方案一的理由是:①节约能源(不需加热),②操作安全简便.
故答案为:
方案一①H2SO4+CuO=CuSO4+H2O; 方案二②H2+CuO=Cu+H2O
一条优点:可节约能源,可少浪费一些资源
点评:本题考查了获取金属的方法的实验方案的设计,完成此题,可以依据已有的物质间的反应规律等知识进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列操作中,正确的是( )
| A、用燃着的酒精灯引燃另一酒精灯 |
| B、用量筒量取液体时,视线要跟量筒内液面的最高处保持水平 |
| C、试管、燃烧匙、蒸发皿都可以直接在酒精灯的火焰上加热 |
| D、称量物放在托盘天平的右盘 |
某同学用仰视读数的方法量取了8mL水,则所量取的水的实际体积是( )
| A、等于8mL | B、大于8mL |
| C、小于8mL | D、无法确定 |
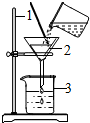 如图为某学生正做粗盐提纯的过滤.操作,试回答:
如图为某学生正做粗盐提纯的过滤.操作,试回答: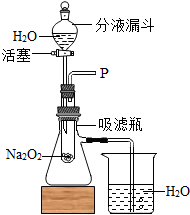 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究.
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究.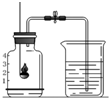 使用红磷燃烧的方法测定空气中氧气的含量:
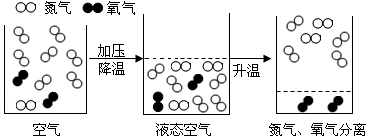
使用红磷燃烧的方法测定空气中氧气的含量: