题目内容
请根据如图所示的实验过程和提供的数据,解答下列问题: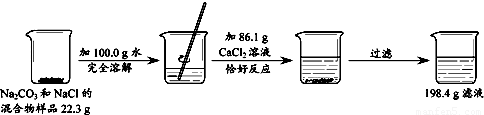
(1)实验过程中的一个明显实验现象是 .
(2)过滤得到的固体物质质量是 g.
(3)试通过计算,求样品中钠元素的质量是多少?(写出相应计算过程)
【答案】分析:依据过程中物质的质量变化利用质量守恒定律求出生成的沉淀质量,然后利用化学方程式求出原混合物中碳酸钠的质量,则可得氯化钠的质量,进而利用化学式的计算可求出钠元素的质量,据此分析解答即可;
解答:解:(1)由于碳酸钠和氯化钙能够反应生成碳酸钙的白色沉淀,所以该过程的明显现象是有白色沉淀生成;
(2)根据质量守恒定律结合题给的数据可以知道生成碳酸钙的质量为:22.3g+100.0g+86.1g-198.4g=10.0g,所以可以据此进行求算;
(3)设混合物中碳酸钠的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.0g
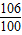 =
=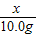
解得:x=10.6g
所以混合物中氯化钠的质量为22.3g-10.6g=11.7g;
所以在混合物中钠元素的质量为:10.6g×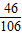 +11.7g×
+11.7g×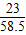 =4.6g+4.6g=9.2g;
=4.6g+4.6g=9.2g;
答:样品中钠元素的质量为9.2g.
故答案为:(1)生成了白色沉淀;(2)10;(1)9.2g;
点评:本题中考查的知识点较多,主要是依据化学方程式进行计算,在解答时要注意运用质量守恒定律来得出计算所必须的已知量,然后依据化学方程式进行计算,同时要学会求算物质中元素的质量.
解答:解:(1)由于碳酸钠和氯化钙能够反应生成碳酸钙的白色沉淀,所以该过程的明显现象是有白色沉淀生成;
(2)根据质量守恒定律结合题给的数据可以知道生成碳酸钙的质量为:22.3g+100.0g+86.1g-198.4g=10.0g,所以可以据此进行求算;
(3)设混合物中碳酸钠的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.0g
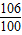 =
=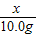
解得:x=10.6g
所以混合物中氯化钠的质量为22.3g-10.6g=11.7g;
所以在混合物中钠元素的质量为:10.6g×
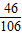 +11.7g×
+11.7g×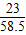 =4.6g+4.6g=9.2g;
=4.6g+4.6g=9.2g;答:样品中钠元素的质量为9.2g.
故答案为:(1)生成了白色沉淀;(2)10;(1)9.2g;
点评:本题中考查的知识点较多,主要是依据化学方程式进行计算,在解答时要注意运用质量守恒定律来得出计算所必须的已知量,然后依据化学方程式进行计算,同时要学会求算物质中元素的质量.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
 .
.


