题目内容
7.下列各组物质充分反应后,溶液总质量变大的是( )| A. | 向澄清石灰水中通入少量二氧化碳 | |
| B. | 向碳酸钠溶液中滴加石灰水 | |
| C. | 石灰石与稀盐酸 | |
| D. | 向过氧化氢溶液中放入少量二氧化锰 |
分析 在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.这就叫做质量守恒定律.据此对选项逐一分析,即可正确选择.
解答 解:A、向澄清石灰水中通入少量二氧化碳,生成了碳酸钙沉淀,溶液的总质量减少,故A不适合;
B、向碳酸钠溶液中滴加石灰水,生成了碳酸钙沉淀,故溶液总质量减少.故B不适合;
C、石灰石与稀盐酸生成了氯化钙、水和二氧化碳,参加反应的碳酸钙的质量大于生成的二氧化碳的质量,反应后溶液的总质量变大,故C适合;
D、向过氧化氢溶液中放入少量二氧化锰.过氧化氢分解放出了氧气,溶液的总质量减少,故D不适合.
故选C.
点评 本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.

练习册系列答案
相关题目
15.A、B、C、D表示4种物质,其微观示意图见表.A和B在一定条件下反应可生成C和D.回答下列问题:
(1)用化学方程式表示上述反应:2NO+2CO$\frac{\underline{\;一定条件\;}}{\;}$2CO2+N2
(2)上述反应中,生成物质C、D等个数比是2:1.
(3)从微观角度解释:化学反应中质量守恒的原因反应前后原子种类、数目均不变.
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  |  |  | |
(2)上述反应中,生成物质C、D等个数比是2:1.
(3)从微观角度解释:化学反应中质量守恒的原因反应前后原子种类、数目均不变.
2.物质的性质决定物质的用途;下列物质的用途与其性质不相符的是( )
| A. | 金刚石用于切割玻璃---------硬度大 | |
| B. | 二氧化碳用于灭火-------既不燃烧也不支持燃烧且密度大于空气 | |
| C. | 活性炭除去冰箱内异味--------吸附性 | |
| D. | 一氧化碳用于工业炼铁---------可燃性 |
19.下列及其解释不相符的是( )
| A. | 金属镁比木炭在空气中燃烧更剧烈------可燃物的性质不同 | |
| B. | 铁丝在空气中不能燃烧,在氧气中能够剧烈燃烧-------氧气含量不同 | |
| C. | 蜂窝煤比煤块在空气中燃烧更剧烈------与氧气接触面积不同 | |
| D. | 火柴头向下比向上放置燃烧个剧烈-------火柴头向上放置与氧气接触面积小 |
4.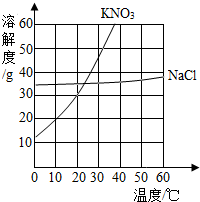 下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:
下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:
(1)P点的含义是23℃时,硝酸钾、氯化钠的溶解度相等.
(2)40℃时,将70g KNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g,该溶液的溶质质量分数是39%.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的基体.
 下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:
下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:| 温度 | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
(2)40℃时,将70g KNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g,该溶液的溶质质量分数是39%.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的基体.

