题目内容
2.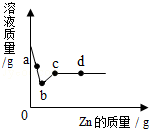 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )| A. | a点溶液中的溶质有3种 | |
| B. | c点溶液中溶质为Cu(NO3)2 | |
| C. | b点溶液中溶质为Zn(NO3)2、Cu(NO3)2 | |
| D. | 取d点的固体,加入稀盐酸,无气泡产生 |
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过各反应的关系进行溶液质量的变化分析.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程
A、在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是三种,故A正确;
B、c点溶液中溶质为Zn(NO3)2,故B错误;
C、b点是硝酸银恰好被反应完,所以b点溶液中溶质为Zn(NO3)2、Cu(NO3)2,故C正确;
D、d点时锌过量,取d点的固体,加入稀盐酸,有气泡产生,故D错误.
故选:AC.
点评 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
19.有200g质量分数是10%的NaOH溶液,若要使它的质量分数增大一倍,不可采用的方法是( )
| A. | 蒸发水100g | B. | 加水使溶液的质量增大一倍 | ||
| C. | 加NaOH固体25g | D. | 加200g质量分数为30%的NaOH溶液 |
12.元素观是化学的重要观念之一,下列有关元素的说法中错误的是( )
| A. | 同种元素在同种化合物中可以显示不同的化合价 | |
| B. | 同种元素的原子核内质子数与中子数一定相等 | |
| C. | 元素周期表,元素的原子序数与该元素元案子核电荷数在数值上相同 | |
| D. | 在物质发生化学变化时,原子的种类不变,元素也不会改变 |




