题目内容
14.小明向量筒中注入水,仰视读数为10mL,倒出一部分水后,俯视读数为7mL,则他倒出来的水的体积是( )| A. | 等于3mL | B. | 大于3mL | C. | 小于3mL | D. | 无法判断 |
分析 根据量筒的使用方法考虑本题,在用量筒量取液体时,接近刻度后要改用胶头滴管,读数时不能仰视或俯视,视线要与凹液面最低处保持水平.
解答 解:仰视液体,看到的读数偏小,但量取的实际液体偏大,所以仰视读数为10毫升,液体的实际体积大于10毫升,俯视液体,看到的读数偏大,但量取的实际体积正好偏小,所以俯视,读数为7毫升,剩余液体的实际体积小于7毫升,所以倒出的液体体积一定大于3毫升.
故选B.
点评 通过回答本题要熟悉常见仪器的使用方法,如果错误操作会造成严重的误差和错误操作带来的危险.

练习册系列答案
相关题目
4.下列化学用语中,既能表示一种元素,又能表示一种物质的是( )
| A. | H2 | B. | Cu | C. | O | D. | 2He |
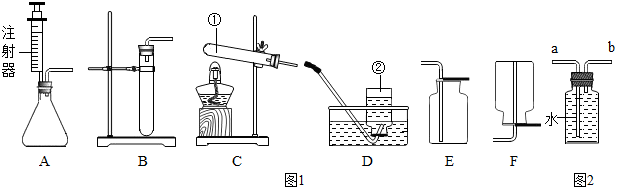
5. 用如图所示装置,在常温下分别进行研究燃烧条件和研究氧气性质的实验.
用如图所示装置,在常温下分别进行研究燃烧条件和研究氧气性质的实验.
已知:白磷的着火点为40℃.
(1)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是 温度未达到白磷的着火点、白磷未与氧气接触;推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧.
(2)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是能支持燃烧;木炭熄灭后冷却一段时间,观察到的现象是烧杯中的部分氢氧化钙溶液进入集气瓶.
 用如图所示装置,在常温下分别进行研究燃烧条件和研究氧气性质的实验.
用如图所示装置,在常温下分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.
| 内容 步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
| I | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中的导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有 Ca(OH)2溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入集气瓶中,塞紧瓶塞 |
| II | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(2)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是能支持燃烧;木炭熄灭后冷却一段时间,观察到的现象是烧杯中的部分氢氧化钙溶液进入集气瓶.
6.长久使用的热水瓶底部有一层水垢.为了除去热水瓶底部的水垢,研究性学习小组的同学进行了下列研究和实验:
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如表:
【分析与研究】
(1)分析表中记录的数据,你认为反应时间为8min时记录的质量数据是错误的.
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为12:16:1.Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与7.3g HCl含有的氯元素的质量相当.
(4)水垢中碳酸钙的质量分数是多少?(请保留计算过程)
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如表:
| 反应时间(min) | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
| m(g) | 294.5 | 290.0 | 286.0 | 286.0 | 283.0 | 282.4 | 282.4 | 282.4 |
(1)分析表中记录的数据,你认为反应时间为8min时记录的质量数据是错误的.
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为12:16:1.Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与7.3g HCl含有的氯元素的质量相当.
(4)水垢中碳酸钙的质量分数是多少?(请保留计算过程)
3.一氧化碳和二氧化碳的相同点是( )
| A. | 利于动植物生长 | B. | 都能还原氧化铜 | ||
| C. | 都能燃烧 | D. | 都是无色的氧化物 |
4.如图表示的反应中,相同的球代表相同的原子,下列说法正确的是( )
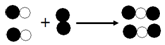
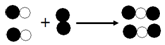
| A. | 原子是化学变化中的最小粒子 | B. | 分子在化学变化中不可分 | ||
| C. | 生成物是混合物 | D. | 该反应是分解反应 |