题目内容
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.
回答下列问题:
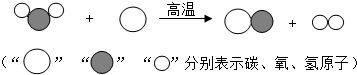
(1)“造气”过程的微观示意图如下,则制备合成气的化学方程式为______ CO+H2↑
【答案】分析:(1)利用图示中相关的物质的结构判断其化学式并书写出相关的方程式,并依据方程式的特点判断其反应类型.
(2)由于合成气是氢气与一氧化碳均具有还原性都能置换出氧化铁中的铁书写相关的方程式.
(3)依据质量守衡定律的应用解答此题.
解答:解:(1)由图示可知反应前是水的分子与碳原子反应后是一氧化碳的分子与氢气分子,由于反应是在高温下进行,此时反应物水为蒸汽,所以生成气体不加气体符号.
可书写出化学方程式为:C+H2O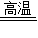 CO+H2↑,该反应的反应物与生成物都是一种单质和一种化合物,所以是置换反应;
CO+H2↑,该反应的反应物与生成物都是一种单质和一种化合物,所以是置换反应;
(2)氢气与一氧化碳均具有还原性都能置换出氧化铁中的铁,同时生成水和二氧化碳,结合方程式的书写解决即可.其方程式为3H2+Fe2O3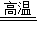 2Fe+3H2O 或 3CO+Fe2O3
2Fe+3H2O 或 3CO+Fe2O3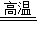 2Fe+3CO2;
2Fe+3CO2;
(3)由质量守恒定律可知化学反应前后元素的种类不变,可知反应前元素有三种即碳氢氧,反应后不会出现氮元素,所以尿素不可能产生.
故答案为:(1)C+H2O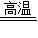 CO+H2↑;置换;(2)3H2+Fe2O3
CO+H2↑;置换;(2)3H2+Fe2O3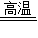 2Fe+3H2O (或 3CO+Fe2O3
2Fe+3H2O (或 3CO+Fe2O3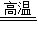 2Fe+3CO2)(3)②;
2Fe+3CO2)(3)②;
点评:此题是对具体的能源利用的考查,解题的关键是发现并找到题目与所学信息的结合点,难度不大知识基础,但开放性较强.
(2)由于合成气是氢气与一氧化碳均具有还原性都能置换出氧化铁中的铁书写相关的方程式.
(3)依据质量守衡定律的应用解答此题.
解答:解:(1)由图示可知反应前是水的分子与碳原子反应后是一氧化碳的分子与氢气分子,由于反应是在高温下进行,此时反应物水为蒸汽,所以生成气体不加气体符号.
可书写出化学方程式为:C+H2O
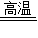 CO+H2↑,该反应的反应物与生成物都是一种单质和一种化合物,所以是置换反应;
CO+H2↑,该反应的反应物与生成物都是一种单质和一种化合物,所以是置换反应;(2)氢气与一氧化碳均具有还原性都能置换出氧化铁中的铁,同时生成水和二氧化碳,结合方程式的书写解决即可.其方程式为3H2+Fe2O3
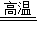 2Fe+3H2O 或 3CO+Fe2O3
2Fe+3H2O 或 3CO+Fe2O3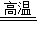 2Fe+3CO2;
2Fe+3CO2;(3)由质量守恒定律可知化学反应前后元素的种类不变,可知反应前元素有三种即碳氢氧,反应后不会出现氮元素,所以尿素不可能产生.
故答案为:(1)C+H2O
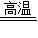 CO+H2↑;置换;(2)3H2+Fe2O3
CO+H2↑;置换;(2)3H2+Fe2O3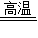 2Fe+3H2O (或 3CO+Fe2O3
2Fe+3H2O (或 3CO+Fe2O3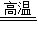 2Fe+3CO2)(3)②;
2Fe+3CO2)(3)②;点评:此题是对具体的能源利用的考查,解题的关键是发现并找到题目与所学信息的结合点,难度不大知识基础,但开放性较强.

练习册系列答案
相关题目
 利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如右图所示.回答下列问题:
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如右图所示.回答下列问题:

 利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题:
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题:
