题目内容
 如图为某种补锌口服液说明书的一部分,请回答:
如图为某种补锌口服液说明书的一部分,请回答:(1)葡萄糖酸锌中含有
(2)一个葡萄糖酸锌分子中含有
(3)葡萄糖酸锌中碳、氢、氧、锌的原子个数比为
(4)葡萄糖酸锌的相对分子质量为
(5)葡萄糖酸锌中碳、氢、氧元素的质量比为
(6)葡萄糖酸锌中氢元素的质量分数为
(7)91克葡萄糖酸锌中含碳元素的质量为
(8)
(9)每支口服液中锌的质量分数为
(10)若儿童1kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半;体重为20kg的儿童每天还须服该口服液
考点:化学式的书写及意义,相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学用语和质量守恒定律
分析:根据物质的化学式的意义以及有关化学式的相关计算类型分析依次解答.
解答:解:(1)由葡萄糖酸锌的化学式C12H22O14Zn可知,它是由碳、氢、氧、锌四种元素组成的;故答案为:四;
(2)根据葡萄糖酸锌的化学式C12H22O14Zn可知,1个葡萄糖酸锌分子中含有12个碳原子、22个氢原子、14个氧原子和1个锌原子,共49个原子;故答案为:49;
(3)根据葡萄糖酸锌的化学式C12H22O14Zn可知,葡萄糖酸锌中碳、氢、氧、锌的原子个数比为:12:22:14:1;故答案为:12:22:14:1;
(4)葡萄糖酸锌的相对分子质量是12×12+1×22+16×14+65=455;故答案为:455;
(5)葡萄糖酸锌中碳、氢、氧元素的质量比=12×12:1×22:16×14=144:22:224=72:11:112;故答案为:72:11:112;
(6)根据化合物中元素的质量分数=
×100%,可知葡萄糖酸锌中氢元素的质量分数为:
×100%≈4.8%;故答案为:4.8%;
(7)91克葡萄糖酸锌中含碳元素的质量为:91g×
×100%=28.8g;故答案为:28.8g;
(8)含有56克氧元素需要葡萄糖酸锌的质量为:56g÷
×100%=113.75g;故答案为:113.75;
(9)根据标签信息可知,每支口服液中锌的质量分数为:
×100%=0.05%;故答案为:0.05%;
(10)儿童1kg体重每日需要0.5mg锌,体重为20kg的儿童每日需要锌=0.5mg×
=10mg;其中一半由口服液提供,则每日需要通过该口服液补充锌5mg;根据标签可知,每支口服液含锌为5mg,所以该儿童每天还须服该口服液1支.故答案为:1.
(2)根据葡萄糖酸锌的化学式C12H22O14Zn可知,1个葡萄糖酸锌分子中含有12个碳原子、22个氢原子、14个氧原子和1个锌原子,共49个原子;故答案为:49;
(3)根据葡萄糖酸锌的化学式C12H22O14Zn可知,葡萄糖酸锌中碳、氢、氧、锌的原子个数比为:12:22:14:1;故答案为:12:22:14:1;
(4)葡萄糖酸锌的相对分子质量是12×12+1×22+16×14+65=455;故答案为:455;
(5)葡萄糖酸锌中碳、氢、氧元素的质量比=12×12:1×22:16×14=144:22:224=72:11:112;故答案为:72:11:112;
(6)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
| 1×22 |
| 455 |
(7)91克葡萄糖酸锌中含碳元素的质量为:91g×
| 12×12 |
| 455 |
(8)含有56克氧元素需要葡萄糖酸锌的质量为:56g÷
| 16×14 |
| 455 |
(9)根据标签信息可知,每支口服液中锌的质量分数为:
| 5mg |
| 10g |
(10)儿童1kg体重每日需要0.5mg锌,体重为20kg的儿童每日需要锌=0.5mg×
| 20kg |
| 1kg |
点评:本题考查根据化学式进行计算以及由标签获得重要信息进行解题的能力,物质的化学式、组成成分、各成分的含量等等是解决标签类问题的基础.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
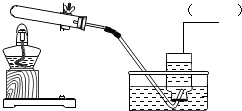 实验室常用氯酸钾和二氧化锰混合加热制取氧气,如图是制取氧气的部分装置图,请回答.
实验室常用氯酸钾和二氧化锰混合加热制取氧气,如图是制取氧气的部分装置图,请回答.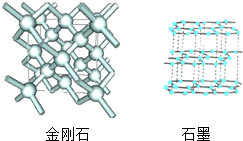 如图分别是金刚石与石墨的分子结构示意图,请通过比较分析,回答下列问题:
如图分别是金刚石与石墨的分子结构示意图,请通过比较分析,回答下列问题:
 如图所示关系图,其中“--”表示相互反应,“→”表示转化关系.
如图所示关系图,其中“--”表示相互反应,“→”表示转化关系.