题目内容
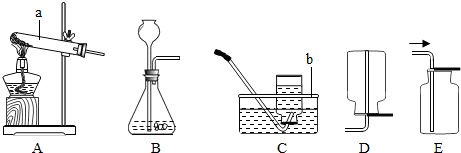
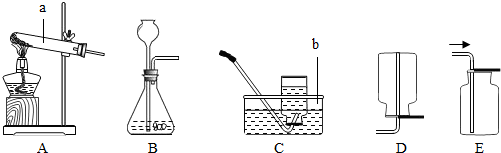
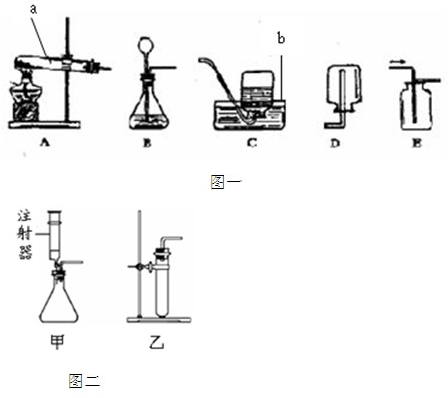
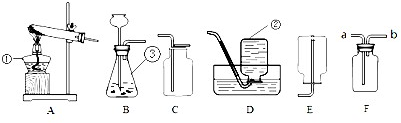
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探险究,以下是他们探究的主要过程:一、假设:H2O2生成O2的快慢与催化剂的种类有关
二、实验方案:常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和红砖粉,测量各收集一瓶(相同体积)O2所需要的时间.
三、实验记录:
| 实验编号 | 1 | 2 |
| 反应物 | 6%H2O2 | 6%H2O2 |
| 催化剂 | 1g红砖粉 | 1gMnO2 |
| 时间 | 152s | 35s |
五、反思:H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验证明它们在化学反应前后的 是否改变.
六、猜想:H2O2生成O2的快慢还与哪些因素有关?(要求提出假设和实验方案,任意一种即可)
【答案】分析:本实验是对催化剂的探究实验,题目中通过控制变化来丰富了催化剂的定义,就是不同的催化剂有不同的催化效果,最终延伸推导还有什么因素能够影响到反应的速率,在这里后期的实验设计可以围绕催化剂的问题展开,也可以围绕反应的控制来进行.
解答:解:题目提出的假设是过氧化氢的分解速率与催化剂的种类有关,相当于先承认了红砖粉和MnO2是该反应的催化剂.所以在后期的验证实验中只需要对比这两种物质的催化效果就可以.而催化效果是通过生成相同量的氧气所用时间来验证的,所以在实验设计中就要严格控制其他的量保持相同(相同质量分数的相同体积的过氧化氢溶液、反应温度相同、制取的氧气的量要相同),因为是验证与种类的关系,所以所取的两种催化剂也是质量相同,最好都是相同的粉末状态.这也是后面我们设计实验时注意的问题.
(1)该探究实验得到的结论:分析这样的问题,一定要从实验的数据中需求问题的解决.实验中除了催化剂的种类不同就是所用时间不同,这就建立起了催化剂种类与反应速率之间的关系,当然就可以下结论:催化剂不同,催化的效果不同.(至于是否都在加快反应,这个问题没有不含催化剂的实验组的对比,就不要盲目下结论).
(2)对于红砖粉和二氧化锰是否是催化剂,在改变反应速率的情况下,就要紧扣催化剂的定义:一个改变(速率)两个不变(质量和化学性质)来分析.这需要通过进一步实验来论证.
(3)题目让我们分析影响过氧化氢的因素,从催化剂可以分析(催化剂的种类、催化剂的质量、催化剂的状态等),也可以从过氧化氢本身(过氧化氢的质量分数),还有就是反应的温度条件等.这些都可以设计实验来验证分析探究.设计时注意我们分析的变量控制,除了要探究的因素外,其余要保持完全一致.这里提供的参考方案是研究催化剂的量对反应的影响的,不是全面的,大家可以再思考,可以考虑增加对比、可以考虑是否催化剂越多越好这样的问题验证.
故答案:
四、H2O2生成氧气的速率与催化剂的种类有关,不同的催化剂催化效果不同..
五、质量、化学性质.
六、假设:H2O2的分解速度与反应物的质量分数有关、催化剂的质量有关、催化剂的状态有关或者和反应的温度有关.(设计实验是验证探究H2O2的分解速率与催化剂的质量有关来设计)
实验方案:在常温下,在两瓶相同体积的相同质量分数的H2O2溶液中加入同样都是粉末的但是质量不同的MnO2测定收集一瓶(相同体积)氧气所需要的时间.
实验记录:
该探究过程得出的结论是:
点评:实验设计中要注意对所有变量在过程中的有效控制,这样会实验结果更有说服力.注意语言和操作的严谨.
解答:解:题目提出的假设是过氧化氢的分解速率与催化剂的种类有关,相当于先承认了红砖粉和MnO2是该反应的催化剂.所以在后期的验证实验中只需要对比这两种物质的催化效果就可以.而催化效果是通过生成相同量的氧气所用时间来验证的,所以在实验设计中就要严格控制其他的量保持相同(相同质量分数的相同体积的过氧化氢溶液、反应温度相同、制取的氧气的量要相同),因为是验证与种类的关系,所以所取的两种催化剂也是质量相同,最好都是相同的粉末状态.这也是后面我们设计实验时注意的问题.
(1)该探究实验得到的结论:分析这样的问题,一定要从实验的数据中需求问题的解决.实验中除了催化剂的种类不同就是所用时间不同,这就建立起了催化剂种类与反应速率之间的关系,当然就可以下结论:催化剂不同,催化的效果不同.(至于是否都在加快反应,这个问题没有不含催化剂的实验组的对比,就不要盲目下结论).
(2)对于红砖粉和二氧化锰是否是催化剂,在改变反应速率的情况下,就要紧扣催化剂的定义:一个改变(速率)两个不变(质量和化学性质)来分析.这需要通过进一步实验来论证.
(3)题目让我们分析影响过氧化氢的因素,从催化剂可以分析(催化剂的种类、催化剂的质量、催化剂的状态等),也可以从过氧化氢本身(过氧化氢的质量分数),还有就是反应的温度条件等.这些都可以设计实验来验证分析探究.设计时注意我们分析的变量控制,除了要探究的因素外,其余要保持完全一致.这里提供的参考方案是研究催化剂的量对反应的影响的,不是全面的,大家可以再思考,可以考虑增加对比、可以考虑是否催化剂越多越好这样的问题验证.
故答案:
四、H2O2生成氧气的速率与催化剂的种类有关,不同的催化剂催化效果不同..
五、质量、化学性质.
六、假设:H2O2的分解速度与反应物的质量分数有关、催化剂的质量有关、催化剂的状态有关或者和反应的温度有关.(设计实验是验证探究H2O2的分解速率与催化剂的质量有关来设计)
实验方案:在常温下,在两瓶相同体积的相同质量分数的H2O2溶液中加入同样都是粉末的但是质量不同的MnO2测定收集一瓶(相同体积)氧气所需要的时间.
实验记录:
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g MnO2 | 0.1g MnO2 |
| 时间(s) |
点评:实验设计中要注意对所有变量在过程中的有效控制,这样会实验结果更有说服力.注意语言和操作的严谨.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目